CorSalud 2014 Jul-Sep;6(3):259-265
CASO CLÍNICO
VARIABILIDAD CLÍNICA, IMAGENOLÓGICA Y QUIRÚRGICA DEL PSEUDOANEURISMA POSQUIRÚRGICO DE LA AORTA ASCENDENTE. INFORME DE TRES CASOS
MSc. Dr. Osvaldo Valdés-Dupeyróna, Dr. Manuel Nafeh-AbizRecka, Dr. Alejandro Villar-Inclána, Dra. Raiza Hernandez-Núñeza, Dr. Rolando N. Carballo-Hidalgoa, Lic. Katina Rodríguez-Reya y MSc. Dr. Jean L. Chao Garcíab
______________
Servicio de Cirugía Cardiovascular. Hospital "Hermanos Ameijeiras". La Habana, Cuba.
Servicio de Cirugía Cardiovascular. Centro de Investigaciones Médico-Quirúrgicas. La Habana, Cuba.
Correspondencia: O Valdés Dupeyrón. Edificio 331, Apto. 22. Rpto. Camilo Cienfuegos. Habana del Este, CP 11700. La Habana, Cuba. Correo electrónico: osvaldovaldes@infomed.sld.cu
Resumen
Los pseudoaneurismas posquirúrgicos de la aorta ascendente presentan un cuadro clínico muy variado, y se manifiestan desde una forma asintomática hasta un cuadro tóxico infeccioso grave o la rotura. También expresan diversidad en cuanto a localización, tiempo de aparición posterior a la primera cirugía y hallazgos quirúrgicos. Se presentan tres casos operados en el Servicio de Cirugía Cardiovascular del Hospital "Hermanos Ameijeiras", en un período de cuatro años. El primero es un paciente operado de comunicación interauricular que días después de su cierre quirúrgico comenzó con un cuadro febril. El segundo caso es una paciente que tres meses posteriores a una cirugía de sustitución valvular aórtica se diagnostica el pseudoaneurisma, donde se recoge, como único antecedente, cuadros febriles a repeticiones; y el tercero, es un enfermo que había sido intervenido de coartación aórtica y al año siguiente, de reemplazo de la valvula aórtica; 17 años más tarde comenzó con dolor precordial, astenia y pérdida de conciencia. Los pseudoaneurismas posquirúrgicos aórticos constituyen un desafío para todos los servicios de cardiología y cirugía cardiovascular, pues muestran gran variedad en sus formas de presentación clínico-quirúrgicas.
Palabras clave: Pseudoaneurisma, Aorta ascendente, Variabilidad clínica, Tratamiento quirúrgico
Clinical, imaging and surgical variability of postoperative pseudoaneurysm of the ascending aorta: Report of three cases
Abstract
The postoperative pseudoaneurysms of the ascending aorta present varied clinical symptoms, and range from asymptomatic forms to severe toxic infectious cases or a rupture. They also show diversity with regard to location, time of occurrence after the first surgery and surgical findings. Three cases of patients who underwent surgery at the Department of Cardiovascular Surgery of the Hermanos Ameijeiras Hospital over a four-year period are reported. The first case is that of a patient who underwent atrial septal defect surgery and days after the surgical closure presented with a fever. The second case was a patient who was diagnosed with pseudoaneurysm three months after an aortic valve replacement surgery, with the only antecedent of repeated febrile episodes; and the third is a patient who had undergone aortic coarctation surgery and the following year underwent aortic valve replacement, then, 17 years later, presented with chest pain, fatigue and loss of consciousness. The postoperative aortic pseudoaneurysms are a challenge for all cardiology and cardiovascular surgery departments as they show a great variety in their forms of clinical-surgical presentation.
Key words: Pseudoaneurysm, Ascending aorta, Clinical variability, Surgical treatment
Introducción
Los pseudoaneurismas (PSA) posquirúrgicos de la aorta ascendente constituyen una grave complicación de la cirugía cardiovascular. A pesar de su baja incidencia, su diagnóstico debe ser preciso por la elevada mortalidad que presentan.
La arteria aorta, pese a la delgadez de su pared, puede resistir sin romperse una presión de miles de milímetros de mercurio. Sin embargo, cuando se daña su integridad en la cirugía cardíaca, los procedimientos endovasculares diagnósticos y terapéuticos1, así como en los traumatismos torácicos abiertos y cerrados, puede provocar —de forma directa o indirecta– lesiones en alguna de las capas de la aorta, lo que conlleva a la formación de aneurismas, disecciones o roturas2-4. El principal mecanismo en la génesis del falso aneurisma es la disrupción de alguna de las capas del vaso, que es contenida por el resto de las capas y estructuras adyacentes, con o sin desarrollo de la neoíntima. Las localizaciones más frecuentes son: la línea de cicatriz de la aortotomía, los sitios de canulación aórtica, de cardioplejia y de pinza de paro, las anastomosis de prótesis vasculares e injertos venosos y, con menor frecuencia, en las suturas aórticas postransplante cardíaco, y en las endocarditis infecciosas de las prótesis valvulares5-8.
El origen infeccioso primario de la aorta es muy raro, aunque se describen casos de afectación vascular por contigüidad o por diseminación hematógena, principalmente en aortas previamente enfermas, lo que puede producir una pequeña perforación transmural, con formación de un hematoma que constituye la pared del PSA8,9. Generalmente esta infección se debe a procesos sépticos en aneurismas preexistentes, diseminación de una endocarditis bacteriana valvular aórtica o de materiales protésicos que han sufrido infección. Estos aneurismas llamados micóticos pueden ser originados por infinidad de gérmenes patógenos, no solamente hongos, y son generalmente, de formación y crecimiento rápido por la debilidad de la pared aórtica9.
Se presentan tres pacientes operados con el diagnóstico de PSA de la aorta ascendente en un período de cuatro años (junio del 2004 hasta junio de 2008), en el Servicio de Cirugía Cardiovascular del Hospital "Hermanos Ameijeiras".
Las técnicas quirúrgicas empleadas fueron la resección del pseudoaneurisma con reparación aórtica mediante aortoplastia, con o sin materiales sintéticos, y la sustitución de válvula y raíz aórticas por un conducto valvado, con reimplante de arterias coronarias.
La información se obtuvo a través de la revisión de las historias clínicas, los informes operatorios y las hojas de anestesia y de perfusión de los pacientes en cuestión.
Casos clínicos
Caso 1
Paciente masculino de 37 años de edad, operado en el año 2004 por comunicación interauricular tipo ostium secundum, la cual requirió parche de pericardio autólogo. En el posoperatorio mediato comenzó con fiebre, por lo que se indicaron complementarios. El leucograma mostró predominio de los polimorfonucleares. Los ecocardiogramas transtorácico (ETT) y transesofágico (ETE) sugirieron la posibilidad de dehiscencia del parche por endocarditis. La fiebre desapareció y se decidió egresar al paciente.
Una semana más tarde el enfermo regresa con un cuadro de tos constante, astenia marcada y edema en miembros inferiores. Se indicó radiografía de tórax (Figura 1), donde se observó ensanchamiento del mediastino, no presente en estudios anteriores. Además se realizó ETE de urgencia que mostró aneurisma de la aurícula derecha por dehiscencia del parche de pericardio implantado en la comunicación interauricular. Con este resultado se decidió realizar tomografía axial computarizada (TAC) contrastada (Figura 2), donde se corroboró la existencia de una masa mediastinal por delante del corazón, la cual se originaba en la aorta ascendente, con pase de contraste de la luz hacia la masa. Con el posible diagnóstico de PSA posquirúrgico, se discutió en el colectivo médico y se determinó tratamiento quirúrgico de emergencia.
En el quirófano se disecaron y canularon los vasos femorales, se comenzó la circulación extracorpórea (CEC) y se descendió la temperatura hasta provocar fibrilación ventricular. Se realizó esternotomía media y se encontró un aneurisma séptico de la aorta torácica, a partir de la zona de canulación aórtica de la primera operación.
Después de descartar la posibilidad de aneurisma de aurícula derecha y dehiscencia del parche, se procedió a resecar los elementos del falso aneurisma y reparar la aorta con parche de dacrón. Se retiró la pinza de paro y el corazón inició los latidos espontáneamente. Se separó al paciente de la CEC, con tiempos de pinzamiento aórtico y CEC de 165 y 220 minutos, respectivamente. El enfermo fue extubado tempranamente y tuvo una estancia en la Unidad de Cuidados Intensivos (UCI) de 48 horas, con una evolución favorable.
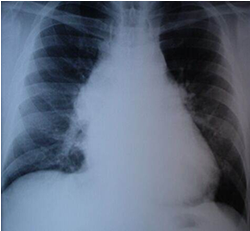
Figura 1. Radiografía póstero-anterior de tórax que muestra ensanchamiento mediastinal.
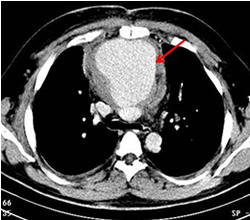
Figura 2. Tomografía helicoidal contrastada que demuestra zona aneurismática a nivel de la aorta ascendente (flecha).
Caso 2
Paciente femenina de 40 años de edad, operada en mayo del 2007 de sustitución valvular aórtica y reintervenida por derrame pericárdico grave, que después de dos meses comenzó con un cuadro febril y no resolvió con tratamiento antibiótico. Por tal motivo se decidió su ingreso para estudio y se realizaron ETT y TAC de mediastino, que diagnosticaron un aneurisma de la aorta ascendente. Un día después se indicó TAC contrastada (Figura 3), que mostró dilatación pseudoaneurismática de la aorta ascendente a nivel supravalvular, que incluía el ostium de la coronaria izquierda y ocupaba el plano anterior y lateral izquierdo; además, se observaba otra masa más pequeña en el plano posterior. Por todo lo expuesto anteriormente se decidió cirugía de urgencia.
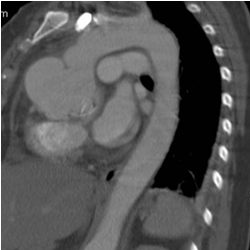
Figura 3. TAC contrastada, con dos sacos aneurismáticos.
En el quirófano se canularon la vena y la arteria femorales. Se disminuyó la temperatura hasta provocar fibrilación ventricular y se realizó esternotomía media. Se disecó el falso aneurisma y se colocó pinza de paro en la aorta ascendente distal al aneurisma, muy próximo a los troncos supraórticos. Se puncionó el PSA y se administró solución cardiopléjica, posteriormente se efectuó la apertura del saco aneurismático y se constató la dehiscencia de la sutura aórtica anterior.
Se exploraron la prótesis valvular y los orificios coronarios, los cuales no estaban incluidos en el falso aneurisma. Se decidió rehacer la sutura anterior, la cual fue reforzada con elementos propios del saco aneurismático. Se retiró la pinza de paro y se produjo latido cardíaco espontáneo, pero a los 10 minutos la paciente presentó fibrilación ventricular, que se trató exitosamente con desfibrilación interna. En el primer intento de salida de la CEC disminuyó la presión arterial, por lo que se indicó baipás de apoyo durante 25 minutos. Se logró suspender la CEC, aunque el paciente necesitó apoyos con dobutamina y epinefrina. Los tiempos de pinzamiento aórtico y de CEC fueron de 106 y 210 minutos, respectivamente. Posteriormente se trasladó a la UCI, donde se extubó a las 14 horas y mantuvo una evolución favorable. La paciente fue egresada a los 30 días, después de concluir el tratamiento antibiótico recomendado.
Caso 3
Paciente masculino de 53 años de edad, con antecedentes de haber sido operado de coartación y sustitución valvular aórticas en el año 1990 y 1991, respectivamente. Acudió a nuestro centro 17 años después por presentar dolor precordial opresivo y pérdida del conocimiento en tres ocasiones. Se ingresó y se indicaron estudios de imágenes. En el ETE se observó dilatación aneurismática de la aorta ascendente que iniciaba en la raíz aórtica inmediatamente a nivel de los senos de Valsalva (raíz aórtica 87 mm), la prótesis mecánica en posición aórtica era normofuncionante, sin fuga periprotésica. En la TAC de tórax se observó PSA de la aorta ascendente que comprometía los senos de Valsalva, la arteria descendente anterior presentaba calcificaciones en su trayecto, pero sin lesiones significativas, y el aneurisma medía 10 x 10 cm en su diámetro mayor. Asimismo, en la TAC contrastada se apreció aneurisma de aorta ascendente que surgía por encima de la prótesis valvular aórtica, e involucraba a los senos coronarios, sin lograr definir el ostium de las arterias coronarias.
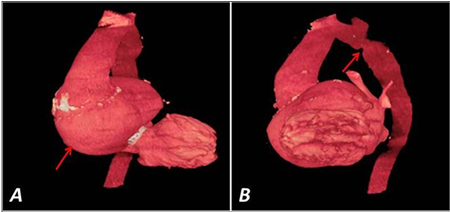
Figura 4. TAC contrastada. A. PSA gigante (flecha) que ocupa los senos de Valsalva y raíz aórtica. B. Además del PSA, se observa coartación residual de la aorta (flecha).
El aneurisma, que medía 95 x 96 x 103 mm, producía marcada compresión de la aurícula izquierda (Figura 4A), y presentaba placas de ateroma calcificadas en su pared lateral derecha. No se evidenciaron signos de disección, ni trombosis asociada. Además, se visualizó coartación de la aorta (Figura 4B), aproximadamente a 15 mm de la emergencia de la subclavia izquierda, con una luz de 14 mm. Con estos resultados se decidió tratamiento quirúrgico urgente.
En el quirófano se realizó canulación fémoro-femoral, se comenzó la CEC, se disminuyó la temperatura hasta provocar fibrilación ventricular y se realizó una esternotomía media. Se encontró PSA gigante inmediato al plano valvular que desplazaba al ventrículo derecho. Se decidió retirar la prótesis, la raíz y parte de la aorta ascendente, y se colocó un tubo valvado número 23, con reimplante del ostium de la coronaria izquierda; además, se revascularizó la arteria coronaria derecha con vena safena. Posteriormente se retiró la pinza de paro y se registró fibrilación ventricular, se realizó desfibrilación interna y apareció ritmo idioventricular, por lo que se colocó un marcapasos y se logró separar de la CEC con apoyo de dobutamina a 7 mcg/kg/minuto. Los tiempos de CEC y pinzamiento aórtico fueron de 350 y 184 minutos, respectivamente.
El enfermo es trasladó a la UCI donde permaneció durante 48 horas y tuvo una evolución posquirúrgica favorable.
Comentario
La variabilidad de los PSA comienza desde su etiopatogenia, aunque la cirugía de sustitución valvular aórtica se mantiene como la causa principal. Mohammadi et al.11 y Atik et al.12 plantean que la formación de PSA después de cirugía aórtica, en presencia de disección, probablemente sea por la fragilidad de los tejidos.
En lo que respecta al cuadro clínico existe una gran diversidad en cuanto a su forma de presentación. Muchos diagnósticos se hacen con exámenes de rutina en pacientes asintomáticos. En un estudio multicéntrico realizado en tres países de Europa13, donde se operaron 43 casos con PSA aórticos, 23 de ellos no tenían síntomas cuando fueron diagnosticados por TAC. Otras series tuvieron un mayor número de casos sintomáticos, y predominaron el dolor torácico y los signos de insuficiencia cardíaca12,14.
En el presente trabajo, los tres pacientes presentaron síntomas sugestivos de la enfermedad, con predominio de la fiebre en dos enfermos. Además, estas afecciones pueden producir manifestaciones respiratorias por compresión y obstrucción bronquial o traqueal y, con menos frecuencia, se puede producir una fístula aorto-bronquial, con hemorragia masiva. También pudieran acompañarse de disfagia por compresión esofágica o hematemesis por fístula aorto-esofágica5-8. De igual modo, cuando su crecimiento es marcado, suelen comprimir otras estructuras como la vena cava superior y la arteria pulmonar, inclusive la pared torácica, lo que dificulta su abordaje quirúrgico posterior15.
En cuanto al tiempo entre la cirugía primaria y el diagnóstico de la enfermedad, los PSA posquirúrgicos pueden manifestarse desde días, meses y hasta años posteriores a la intervención quirúrgica. Malvindi et al.13 tuvieron una media de 98 meses con rango entre 2 y 452 meses. En otras series11,12,14 este período osciló entre 2 y 6 años, aproximadamente.
En el actual trabajo se presentaron tres pacientes, donde la diversidad clínica estuvo muy representada, pues un enfermo debutó con el PSA días después de la intervención; otro, tres meses después y en el tercero, la enfermedad se diagnosticó 17 años pasada la cirugía.
Referente al lugar de formación de los PSA, comentado en la introducción, también existe disimilitud. Los estudios de imágenes constituyen los pilares fundamentales para corroborar el pensamiento clínico en estas situaciones. El ETE, la TAC y la resonancia magnética son los medios diagnósticos más utilizados. En nuestro centro, la TAC constituye el patrón imagenológico en todas las afecciones quirúrgicas de la arteria aorta, independientemente a que se determine el diagnóstico con otra modalidad complementaria16.
El tratamiento de los PSA es exclusivamente quirúrgico, y en su mayoría de extrema urgencia. Uno de los principios que debe tener en cuenta el grupo quirúrgico, previo a la cirugía, es conocer las condiciones anatómicas del PSA, mediante los estudios de imágenes. Posteriormente se traza la estrategia entre anestesiólogo, perfusionista y cirujano, con el objetivo de minimizar la posibilidad de accidentes durante la intervención quirúrgica. Sobre la esternotomía, diversos estudios plantean una serie de variantes5,11,14,16-20, todas en baipás cardiopulmonar, con un grado menor o mayor de hipotermia, con o sin fibrilación ventricular, pero siempre con el propósito de realizar la apertura del tórax en las condiciones más óptimas posibles.
Por otra parte, el empleo del paro circulatorio con canulación de algún vaso supraaórtico para protección cerebral anterógrada es una variante segura en el tratamiento de los PSA aórticos complejos. En nuestro centro se realizan todas las variedades descritas anteriormente. En los últimos diez años se introdujo la canulación de las arterias axilares y carótidas como método de protección cerebral anterógrada, con excelentes resultados.
Las técnicas quirúrgicas empleadas también son diversas y dependen principalmente de las condiciones generales del enfermo y las características morfológicas del PSA. Cuando los tejidos están muy dañados o friables, se debe realizar una técnica sustitutiva radical, como el empleo de prótesis vasculares valvadas o no, siempre que el estado del paciente lo permita. Contrariamente si el falso aneurisma es pequeño, localizado, alejado del plano valvular, con tejidos circundante de aspecto normal, entonces sí debe procederse a realizar una técnica reparadora, con o sin material protésico. Además, nuestro centro trabaja en la incorporación de procedimientos endovasculares, los cuales se han extendido a los PSA de la aorta ascendente desde hace algunos años20-22.
Conclusiones
La variabilidad clínica, imagenológica y quirúrgica de los PSA posquirúrgicos de la aorta ascendente hace que su conducta clínico-quirúrgica sea recomendada al personal médico de mayor experiencia en estas afecciones. El diagnóstico y tratamiento de los PSA incluyen un conjunto de decisiones constantes y seguras, que de no aplicarse correctamente llevan a la ocurrencia de complicaciones o la muerte del paciente.
Referencias bibliográficas
Van der Wal H, Van Geel PP, De Boer RA. Mycotic aneurysm of the aorta as an unusual complication of coronary angiography. Eur J Vasc Endovasc Surg. 2008;36(2):178-81.
Schmoker JD, Miller DC. A simple trick for repairing coronary pseudoaneurysm complicating a Bentall operation. Ann Thorac Surg. 2002;74(1):268-70.
Pomes H, Trainini JC, Volman S, Mauro V, Sampó E, Hershson A, et al. Consenso de patología de la aorta. Rev Argent Cardiol. 2004;72(5):387-401.
Vaccarino GN, Piccinini FF, Nacinovich F, Delli Carpini L, Dorsa A, Navia DO. Seudoaneurisma de la aorta ascendente luego de reemplazo valvular aórtico: una emergencia quirúrgica. Rev Argent Cardiol. 2005;73(4):308-10.
Valdés O, Céspedes G, Mederos B, Pupo P. Pseudoaneurisma de la aorta ascendente después de sustitución valvular aórtica. Medisur [Internet]. 2010 [citado 2011 Ene 12];8(3):[aprox. 3p.]. Disponible en: http://scielo.sld.cu/scielo.php?pid=S1727-897X2010000300013&script=sci_arttext
Gabbieri D, Dohmen PM, Linneweber J, Lembcke A, von Heymann C, Konertz WF. Mycotic pseudoaneurysm of the ascending aorta at site of aortic cannulation. Asian Cardiovasc Thorac Ann. 2008;16(2):e15-7.
Konia M, Uppington J, Moore P, Liu H. Ascending aortic pseudoaneurysm: a late complication of coronary artery bypass. Anesth Analg. 2008;106(3):767-8.
Escribano P, López F, Delgado JF, Sotelo T, Aguado JM, Rodríguez E. Aneurisma micótico en la línea de sutura aórtica tras el trasplante cardíaco. Rev Esp Cardiol. 2000;53(10):1403-5.
Martínez-Vázquez C, Nodar A, Crespo M, Seijas M, Cid D, López A, et al. Pseudoaneurisma micótico por Mycobacterium tuberculosis. An Med Interna. 2001;18(11):594-6.
del Cueto H. Aneurisma disecante de aorta ascendente. MEDISAN [Internet]. 1998 [citado 2011 Ene 12];2(Esp.):30-72. Disponible en: http://bvs.sld.cu/revistas/san/vol2_s_98/esp03198.pdf
Mohammadi S, Bonnet N, Leprince P, Kolsi M, Rama A, Pavie A, et al. Reoperation for false aneurysm of the ascending aorta after its prosthetic replacement: surgical strategy. Ann Thorac Surg. 2005;79(1):147-52.
Atik FA, Navia JL, Svensson L, Vega PR, Feng J, Brizzio ME, et al. Surgical treatment of pseudoaneurysm of the thoracic aorta. J Thorac Cardiovasc Surg. 2006;132(2):379-85.
Malvindi PG, van Putte BP, Heijmen RH, Schepens MA, Morshuis WJ. Reoperations for aortic false aneurysms after cardiac surgery. Ann Thorac Surg. 2010;90(5):1437-43.
Settepani F, Muretti M, Barbone A, Citterio E, Eusebio A, Ornaghi D, et al. Reoperation for aortic false aneurysm: our experience and strategy for safe resternotomy. J Card Surg. 2008;23(3):216 -20.
Bachet J, Pirotte M, Laborde F, Guilmet D. Reoperation for giant false aneurysm of the thoracic aorta: how to reenter the chest? Ann Thorac Surg. 2007;83(5):1610-4.
Valdés Dupeyrón O, Villar Inclán A, Nafeh Abiz-Reck M, Pedroso J, Guevara González L, Chao González N, et al. Tratamiento quirúrgico de las enfermedades de la aorta ascendente. Estudio de tres años. RACCV. 2011;IX (1):47-59.
Kirsch EW, Radu NC, Mekontso A, Hillion ML, Loisance D. Aortic root replacement after previous surgical intervention on the aortic valve, aortic root, or ascending aorta. J Thorac Cardiovasc Surg. 2006;131(3):601-8.
Malvindi PG, van Putte BP, Heijmen RH, Schepens MA, Morshuis WJ. Reoperations on the aortic root: experience in 46 patients. Ann Thorac Surg. 2010;89(1):81-6.
Emaminia A, Amirghofran AA, Shafa M, Moaref A, Javan R. Ascending aortic pseudoaneurysm after aortic valve replacement: watch the tip of the cardioplegia cannula! J Thorac Cardiovasc Surg. 2009;137(5):1285-6.
Dumont E, Carrier M, Cartier R, Pellerin M, Poirier N, Bouchard D, et al. Repair of aortic false aneurysm using deep hypothermia and circulatory arrest. Ann Thorac Surg. 2004;78(1):117-20.
Kannan BR, Jain AK, Qureshi SA, Rothman MT, Rosenthal E, Mathur A. Successful exclusion of large post-surgical pseudoaneurysm of the ascending aorta by a percutaneous approach. Ann Thorac Surg. 2009;87(4):1281-4.
Kpodonu J, Wheatley GH, Ramaiah VG, Rodriguez JA, Strumpf RK, Diethrich EB. Endovascular repair of an ascending aortic pseudoaneurysm with a septal occluder device: mid-term follow-up. Ann Thorac Surg. 2008;85(1):349-51.
Recibido: 24 de enero de 2014
Aceptado: 18 de febrero de 2014
Subir