CorSalud 2014 Ene-Mar;6(1):63-69
ARTÍCULO BREVE
ARRITMIAS VENTRICULARES MALIGNAS EN PACIENTES CON CARDIODESFIBRILADOR IMPLANTABLE: SIGNOS ELÉCTRICOS PREDICTORES DE RECIDIVAS
Dra. Ailema A. Alemán-Fernández, Dra. Margarita Dorantes-Sánchez, Dr.C. Jesús Castro Hevia, Dra. Lisbeth González González, Dr. Yoel Coto Hernández, Dr. Marcos A. Rodríguez García
______________
Instituto de Cardiología y Cirugía Cardiovascular. La Habana, Cuba.
Correspondencia: AA. Alemán Fernández. Calle 17 N° 702, e/ Paseo y A, CP 10400. La Habana, Cuba.
Correo electrónico: aleman@infomed.sld.cu
Resumen
Introducción: Existe un número creciente de pacientes con cardiodesfibriladores, las recidivas son frecuentes y los choques eléctricos constituyen el principal factor reductor de la calidad de vida. Objetivo: Identificar los predictores electrocardiográficos de recidivas de arritmias ventriculares malignas en estos sujetos. Método: De un universo de 76 pacientes a los que se les había implantado un cardiodesfibrilador automático implantable, se seleccionaron 46 y se confeccionaron dos grupos. El A estuvo constituido por 27 pacientes, con al menos un episodio de arritmias ventriculares malignas tras el implante del dispositivo; y el B, por los 19 sujetos sin recurrencias. Las mediciones (QTc prolongado, dispersión anormal del QT, Tpico-Tfinal y su dispersión anormal) se promediaron en tres latidos consecutivos en cada derivación, de forma manual, por dos observadores independientes. Resultados: En el grupo A predominó la cardiopatía estructural y la fracción de eyección inferior a 35 %. Estuvieron igualmente representados la fragmentación del complejo QRS, la onda T bimodal y el patrón de repolarización precoz. Hubo diferencias significativas en los valores medios del intervalo QT (428 vs. 390 ms), p=0.004; del QT corregido (476 vs. 436 ms), p=0.011; y del intervalo Tpico-Tfinal (108 vs. 87 ms), p=0.006. No existieron en la dispersión del QT (51 vs. 48 ms), la dispersión del Tpico-Tfinal (35 vs. 27 ms), ni en la duración del QRS (121 vs. 105 ms). Conclusiones: Los intervalos QT, QTc y Tpico-Tfinal son predictores electrocardiográficos de recidivas de arritmias ventriculares en pacientes con cardiodesfibriladores.
Palabras clave: Cardiodesfibrilador implantable, Predictores eléctricos, Recidivas, Arritmias ventriculares malignas
Malignant ventricular arrhythmias in patients with implantable cardioverter-defibrillators: electrical signals which are predictors of recurrence
Abstract
Introduction: There is a growing number of patients with implantable cardioverter-defibrillators. Recurrences are frequent and electrical shocks are the main factor affecting the quality of life. Objective: To identify the electrocardiographic predictors of the recurrence of malignant ventricular arrhythmias in these patients. Method: From a universe of 76 patients, who had undergone cardioverter-defibrillator implantation, 46 patients were selected and two groups were formed. Group A consisted of 27 patients with at least one episode of malignant ventricular arrhythmias after device implantation; and group B consisted of 19 subjects without recurrences. Measurements (prolonged QTc, abnormal QT dispersion, Tpeak-Tend interval and its abnormal dispersion) were averaged over three consecutive heartbeats in each lead, manually, by two independent observers. Results: In group A, there was a predominance of structural heart disease and an ejection fraction less than 35%. The fragmentation of the QRS complex, bimodal T wave and early repolarization pattern were also present. There were significant differences in the mean values of the QT interval (428 vs. 390 ms), p=0.004; the corrected QT (476 vs. 436 ms), p=0.011; and Tpeak-Tend interval (108 vs. 87 ms), p=0.006. There were no significant differences in QT dispersion (51 vs. 48 ms), the Tpeak-Tend dispersion (35 vs. 27 ms), or QRS duration (121 vs. 105 ms). Conclusions: QT, QTc and Tpeak-Tend intervals are electrocardiographic predictors of the recurrence of ventricular arrhythmias in patients with implantable cardioverter-defibrillators.
Key words: Implantable cardioverter-defibrillator, Electrical predictors, Recurrence, Malignant ventricular arrhythmias
Introducción
Uno de los principales conflictos en los pacientes con cardiodesfibriladores automáticos implantables (CDAI) son los choques eléctricos repetidos. Existen numerosos marcadores relacionados con este fenómeno, muchos de ellos son complejos en su obtención y reproducibilidad. En el electrocardiograma de superficie pueden hallarse signos que reflejan alteraciones en los procesos de despolarización y repolarización ventriculares. Su identificación permitiría establecer una estratificación más certera del riesgo individual, definir una estrategia terapéutica y evitar las complicaciones en pacientes de alto riesgo arrítmico. El objetivo de este trabajo fue identificar los signos electrocardiográficos predictores de recidivas de arritmias ventriculares malignas (AVM) en el seguimiento clínico de pacientes con CDAI.
Método
El universo estuvo conformado por 76 pacientes atendidos en el Servicio de Arritmias y Estimulación Eléctrica del Instituto de Cardiología y Cirugía Cardiovascular, con edades comprendidas entre 15 y 80 años, de ambos sexos, con cardiopatía estructural demostrable o sin ella, a los que se les había implantado un CDAI como prevención secundaria de AVM o primaria (un solo caso). La muestra, definida por el período de estudio (entre febrero del 2007 y febrero del 2009) y los criterios de inclusión (poseer un electrocardiograma basal próximo al suceso arrítmico o a la implantación del dispositivo, sin empleo de fármacos antiarrítmicos), estuvo conformada por 46 pacientes, 34 hombres (73,9 %), en edades entre 40 y 70 años.
Se confeccionaron dos grupos, el A estuvo constituido por 27 pacientes, con al menos un episodio de AVM tras el implante del dispositivo, y el B, lo conformaron 19 sujetos sin recurrencias.
Se definió como recidiva el primer episodio de AVM tras el implante del dispositivo; y para ser incluido en el grupo B, dos años o más de seguimiento sin AVM.
Las mediciones se promediaron en tres latidos consecutivos en cada derivación, de forma manual por dos observadores independientes; los resultados se compararon y se consideró como válido el mayor valor. Si las diferencias eran superiores a 20 ms, se tomó una por acuerdo o se consultó a un tercer experto.
Se emplearon los siguientes conceptos1,2:
QTc prolongado: mayor de 460 ms.
Dispersión anormal del QT (dQT): mayor de 65 ms.
Tpico-Tfinal (Tp-Tf) prolongado: igual o mayor de 100 ms.
Dispersión anormal del Tp-Tf (dTp-Tf): mayor de 20 ms.
Para la comparación de las medidas descriptivas de resumen se calculó media, desviación estándar y porcentaje. En la búsqueda de asociación de variables se utilizó la prueba de Chi cuadrado de Pearson para variables cualitativas, y la prueba t en la comparación de medias entre grupos. Se valoró la supervivencia de los pacientes según los valores del Tp-Tf, mediante el análisis de la curva de Kaplan-Meier3.
Resultados
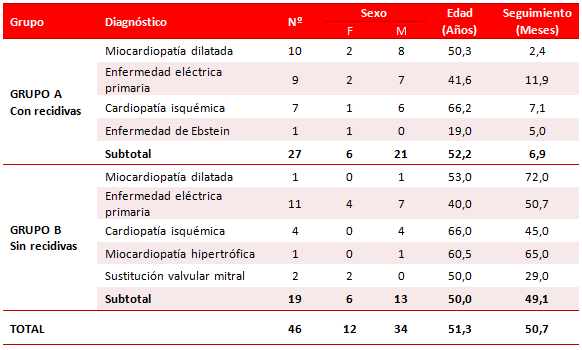
La edad y el sexo se distribuyeron de forma similar en ambos grupos (Tabla 1). En los pacientes con recidivas predominó la presencia de cardiopatía estructural (66,7 %), entre ellas la miocardiopatía dilatada (37 %). En el grupo B, la enfermedad eléctrica primaria (57,8 %).
Tabla 1. Características demográficas, enfermedad de base y tiempo de seguimiento.
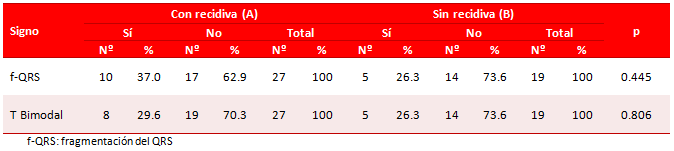
Las variables electrocardiográficas cualitativas (la fragmentación del QRS, la onda T bimodal y el patrón de repolarización precoz) se distribuyeron de forma similar en los dos grupos, aunque predominó levemente la fragmentación del QRS (f-QRS) en el grupo A (Tabla 2).
Tabla 2. Fragmentación del QRS y morfología bimodal de la onda T.
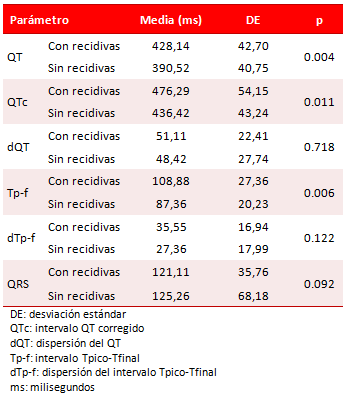
Las variables electrocardiográficas cuantitativas se muestran en la tabla 3. Hubo diferencias estadísticamente significativas en los valores medios de QT, QTc y Tp-Tf entre ambos grupos. No fue así con el resto de los valores, que se comportaron de forma similar (dQT, dTp-f y duración del QRS).
Tabla 3. Distribución de las variables cuantitativas.
La duración del QRS en los pacientes con recidivas, que presentaron tormenta eléctrica, mostraron valores medios significativamente prolongados (128,3 ± 38,6 ms), al compararlos con el grupo sin recidivas (105,7 ± 17,7 ms), p = 0.045.
Discusión
En el Instituto de Cardiología y Cirugía Cardiovascular, centro nacional de referencia de los pacientes con AVM y criterio de implantación de CDAI, se enfrentó el conflicto de las frecuentes recidivas de estos sucesos (incluso en mayor número después de colocado el dispositivo)4,5, la necesidad de utilización de fármacos antiarrítmicos y de la reprogramación del equipo, así como los efectos adversos de los choques repetidos. Resultaba importante acercarse a esta población con mayor riesgo de recidivas, mediante mediciones asequibles y reproducibles, para tomar las medidas adecuadas.
El 58,7 % de los pacientes en esta investigación presentaron recidivas, cifra elevada si se compara con un estudio del mismo centro (115 portadores de CDAI, con recurrencia de AVM en un 31,3 %)5. En otro trabajo4, de 67 pacientes resucitados de muerte súbita (MS) sin anomalía estructural demostrable hubo recidivas en el 74,6 %. Algunos estudios internacionales informan recurrencias entre un 50 y 70 % de los receptores de CDAI en los dos primeros años6-9. Su frecuencia es una realidad y un conflicto a resolver.
Es llamativa la precoz ocurrencia de las recidivas, pues todas se manifestaron en el primer año de seguimiento y en el 37 % durante los tres primeros meses. Ello podría explicarse porque en general, tras el implante, se suspenden los antiarrítmicos y solo se reinstauran después, en caso de ser necesarios. También se han descrito cuestiones inherentes al dispositivo10.
La f-QRS no tuvo diferencias estadísticamente significativas entre los dos grupos, (se encontró en ambos, en 1 de los 8 pacientes con síndrome de Brugada). Morita et al.11, en 115 sujetos con esa canalopatía hallaron f-QRS en el 43 %, con mayor incidencia en aquellos con historia de fibrilación ventricular. Este marcador prevaleció en los pacientes con diagnóstico de cardiopatía isquémica, dilatados y no dilatados, como se describe en la literatura12.
No hubo diferencias en la presencia de la onda T bimodal entre ambos grupos, este parámetro se ha descrito en pacientes con síndrome de QT largo (SQTL)13. Se encontró en 2 de 5 sujetos con dicha enfermedad y en 6 con cardiopatía estructural.
El patrón de repolarización precoz en las derivaciones inferolaterales como predictor de AVM, descrito por otros autores14-16, no se detectó en esta serie.
Los valores medios del QT estuvieron dentro de límites normales en los dos grupos, con diferencias significativas entre los que recurrieron y aquellos que no lo hicieron (Tabla 3). Los valores medios del QTc (Bazett) estuvieron levemente prolongados en el grupo A y mostraron diferencias significativas con el B.
La prolongación del intervalo QT se asocia a un riesgo aumentado de AVM y MS cardíaca en diversas condiciones clínicas que incluyen el SQTL congénito y adquirido, el infarto de miocardio, la miocardiopatía hipertrófica, la hipertensión arterial, los pacientes operados de tetralogía de Fallot, las disfunciones ventriculares e incluso en los sujetos aparentemente sanos17,18-22. El estudio MADIT II encontró asociación entre la prolongación del intervalo QT y la ocurrencia de taquicardia y fibrilación ventriculares espontáneas20. Otras investigaciones han afirmado que la prolongación anormal del QT es un predictor independiente de muerte arrítmica en pacientes postinfarto23-25.
Los valores de dispersión del QT superiores a 60 ms se consideran prolongados y marcadores de riesgo de MS por AVM22-25. Los valores medios de esta serie fueron normales en ambos grupos, sin diferencias significativas. Esto puede justificarse por la variabilidad de los parámetros que reflejan la dispersión de la repolarización en un mismo paciente en diferentes momentos. Si se hubieran medido varios electrocardiogramas basales de cada uno, quizás se habrían encontrado cifras mayores.
Los valores medios del Tp-Tf mostraron diferencias significativas entre los grupos A y B (Tabla 3). El Tp-Tf refleja la dispersión transmural de la repolarización y el consecuente riesgo de AVM. Este parámetro se ha estudiado como predictor de taquiarritmias ventriculares malignas en pacientes con síndrome de Brugada2, SQTL congénito y adquirido, miocardiopatía hipertrófica y cardiopatía isquémica26-28.
En este trabajo se empleó como valor de corte del Tp-f, 100 ms2. El análisis de sobrevivencia (Kaplan-Meier), mostró una diferencia estadísticamente significativa entre las curvas de los pacientes con Tp-Tf ≥ 100 ms y aquellos con cifras menores. La mayoría de los pacientes con valor igual o superior, presentaron “menor supervivencia” o sea, recibieron choques del equipo por AVM. La mayor parte de los sujetos con Tp-Tf inferior a 100 ms no requirieron este tipo de terapia (Figura 1).
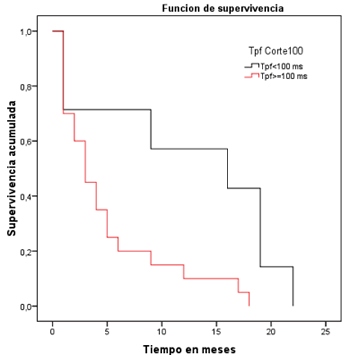
Figura 1. Curva de supervivencia (Kaplan Meier) Tp-Tf.
No existieron diferencias estadísticamente significativas entre la dispersión del Tp-Tf del grupo recurrente y del no recurrente; sin embargo, los valores medios de ambos grupos estuvieron por encima de 27 ms. La dispersión del Tp-Tf refleja las variaciones de la repolarización transmural y es un parámetro que se ha estudiado poco. Castro et al.2 demostraron, en pacientes con síndrome de Brugada, que un punto de corte mayor de 20 ms era predictor de recurrencias. Nuestra muestra incluyó pacientes de alto riesgo (prevención secundaria de MS cardíaca), lo que justifica la presencia de valores elevados en ambos grupos.
La duración media del QRS fue de 121 ms para el grupo A y 105 ms para el B, sin diferencia estadística. Sin embargo, fue capaz de diferenciar de manera significativa el subgrupo de tormenta eléctrica (valores medios por encima de los 120 ms) de los que no presentaron recidivas, lo que refleja una activación transmural anómala. Varios estudios en sujetos con cardiopatía estructural y sin ella han señalado el papel de la prolongación del QRS como marcador de riesgo de MS29,31.
Las recidivas de AVM en pacientes con CDAI son muy frecuentes. Resulta sumamente difícil la estratificación de riesgo: los signos descritos carecen de precisión absoluta en cuanto a sensibilidad y especificidad; su variabilidad es frecuente; el límite real entre los hallazgos “inocentes” y los arritmogénicos no se conoce; sería necesario el análisis de secuencias eléctricas. A lo cual se suma el hecho fundamental de la gran complejidad de los eventos arrítmicos en sí mismos.
En esta investigación los signos electrocardiográficos cuantitativos, como el QT, el QTc y el Tp-Tf, identificaron un subgrupo de pacientes con CDAI con muy alto riesgo de presentar recidivas de AVM, lo cual permitió tomar una conducta adecuada: tratamiento más enérgico de la enfermedad de base, elección del fármaco antiarrítmico, reprogramación del dispositivo y seguimiento más estrecho.
Conclusiones
Los intervalos QT, QTc y Tp-Tf son predictores eléctricos de recidivas de AVM en pacientes con cardiodesfibriladores automáticos implantados.
Referencias bibliográficas
Moss AJ. QTc prolongation and sudden cardiac death: the association is in the detail. J Am Coll Cardiol. 2006;47(2):368-9.
Castro Hevia J, Antzelevitch C, Tornés Bárzaga F, Dorantes Sánchez M, Dorticós Balea F, Zayas Molina R, et al. Tpeak-Tend and Tpeak-Tend dispersion as risk factors for ventricular tachycardia/ventricular fibrillation in patients with the Brugada syndrome. J Am Coll Cardiol. 2006;47(9):1828-34.
Kaplan EL, Meier P. Nonparametric estimation from incomplete observations. J Am Stat Assoc. 1958;53(282):457-81.
Dorantes M, Castro J, Tornés F, Quiñones MA, Zayas R, Dorticós F. Muerte súbita por causa eléctrica en sujetos sin enfermedad cardíaca estructural demostrable. Experiencia cubana. Arch Cardiol Méx. 2004;74(4):283-9.
Tornés FJ, Cisneros P, Dorantes M, Castro J, Zayas R, Quiñones MA, et al. Tormenta eléctrica en pacientes con cardioversor-desfibrilador automático implantable. Arch Cardiol Mex. 2008;78(1):68-78.
Jordaens LJ, Mekel JM. Electrical storm in the ICD era. Europace. 2005;7(2):181-3.
Credner SC, Klingenheben T, Mauss O, Sticherling C, Hohnloser SH. Electrical storm in patients with transvenous implantable cardioverter-defibrillators: incidence, management and prognostic implications. J Am Coll Cardiol. 1998;32(7):1909-15.
Freedberg NA, Hill JN, Fogel RI, Prystowsky EN. Recurrence of symptomatic ventricular arrhythmias in patients with implantable cardioverter defibrillator after the first device therapy: implications for antiarrhythmic therapy and driving restrictions. J Am Coll Cardiol. 2001;37(7):1910-5.
Sánchez JM, Katsiyiannis WT, Gage BF, Chen J, Faddis MN, Gleva MJ, et al. Implantable cardioverter-defibrillator therapy improves long-term survival in patients with unexplained syncope, cardiomyopathy, and a negative electrophysiologic study. Heart Rhythm. 2005;2(4):367-73.
Healy E, Goyal S, Browning C, Robotis D, Ramaswamy K, Rofino-Nadoworny K, et al. Inappropriate ICD therapy due to proarrhythmic ICD shocks and hyperpolarization. Pacing Clin Electrophysiol. 2004;27(3):415-6.
Morita H, Kusano KF, Miura D, Nagase S, Nakamura K, Morita ST, et al. Fragmented QRS as a marker of conduction abnormality and a predictor of prognosis of Brugada syndrome. Circulation. 2008;118(17):1697-704.
Das MK, Zipes DP. Fragmented QRS: a predictor of mortality and sudden cardiac death. Heart Rhythm. 2009;6(3 Suppl):S8-14.
Viitasalo M, Oikarinen L, Swan H, Väänänen H, Glatter K, Laitinen PJ, et al. Ambulatory electrocardiographic evidence of transmural dispersion of repolarization in patients with long-QT syndrome type 1 and 2. Circulation. 2002;106(19):2473-8.
Yan GX, Antzelevitch C. Cellular basis for the electrocardiographic J wave. Circulation. 1996;93(2):372-9.
Wellens HJ. Early repolarization revisited. N Engl J Med. 2008;358(19):2063-5.
Rosso R, Kogan E, Belhassen B, Rozovski U, Scheinman MM, Zeltser D, et al. J-point elevation in survivors of primary ventricular fibrillation and matched control subjects. Incidence and clinical significance. J Am Coll Cardiol. 2008;52(15):1231-8.
Buja G, Miorelli M, Turrini P, Melacini P, Nava A. Comparison of QT dispersion in hypertrophic cardiomyopathy between patients with and without ventricular arrhythmias and sudden death. Am J Cardiol.1993;72(12):973-6.
Shah RR. Drug-induced QT dispersion: does it predict the risk of torsade de pointes? J Electrocardiol. 2005;38(1):10-8.
Gadaleta FL, Llois SC, Sinisi VA, Quiles J, Avanzas P, Kaski JC. Prolongación del intervalo QT corregido: nuevo predictor de riesgo cardiovascular en el síndrome coronario agudo sin elevación del ST. Rev Esp Cardiol. 2008;61(6):572-8.
Moss AJ, Hall WJ, Cannom DS, Daubert JP, Higgins SL, Klein H, et al. Improve survival with an implanted defibrillator in patients with coronary disease at high risk for ventricular arrhythmia. N Engl J Med. 1996;335(26):1933-40.
Aiba T, Shimizu W, Inagaki M, Satomi K, Taguchi A, Kurita T, et al. Excessive increase in QT interval and dispersion of repolarization predict recurrent ventricular tachyarrhythmia after amiodarone. Pacing Clin Electrophysiol. 2004;27(7):901-9.
Malik M, Batchvarov VN. Measurement, interpretation and clinical potential of QT dispersion. J Am Coll Cardiol. 2000;36(6):1749-66.
Perkiömäki JS, Koistinen MJ, Yli-Mäyry S, Huikuri HV. Dispersion of QT interval in patients with and without susceptibility to ventricular tachyarrhythmias after previous myocardial infarction. J Am Coll Cardiol. 1995;26(1):174-9.
Mirvis DM. Spatial variation of QT intervals in normal persons and patients with acute myocardial infarction. J Am Coll Cardiol. 1985;5(3):625-31.
Kelly RF, Parillo JE, Hollenberg SM. Effect of coronary angioplasty on QT dispersion. Am Heart J. 1997;134(3):399-405.
Yamaguchi M, Shimizu M, Ino H, Terai H, Uchiyama K, Oe K, et al. T wave peak-to-end interval and QT dispersion in acquired long QT syndrome: a new index for arrhythmogenicity. Clin Sci (Lond).2003;105(6):671-6.
Antzelevitch C. T peak-Tend interval as an index of transmural dispersion of repolarization. Eur J Clin Invest. 2001;31(7):555-7.
Kors JA, Ritsema van Eck HJ, van Herpen G. The meaning of the Tp-Te interval and its diagnostic value. J Electrocardiol. 2008;41(6):575-80.
Desai AD, Yaw TS, Yamazaki T, Kaykha A, Chun S, Froelicher VF. Prognostic significance of quantitative QRS duration. Am J Med. 2006;119(7):600-6.
Shamim W, Yousufuddin M, Cicoria M, Gibson DG, Coats AJ, Henein MY. Incremental changes in QRS duration in serial ECGs over time identify high risk elderly patients with heart failure. Heart. 2002;88(1):47-51.
Kardys I, Kors JA, van der Meer IM, Hofman A, van der Kuip DA, Witteman JC. Spatial QRS-T angle predicts cardiac death in a general population. Eur Heart J. 2003;24(14):1357-64.
Recibido: 29 de septiembre de 2013
Aceptado: 07 de noviembre de 2013
Subir