CorSalud 2014 Ene-Mar;6(1):11-17
ARTÍCULO ORIGINAL
PREDICTORES ECOCARDIOGRÁFICOS DE DISFUNCIÓN SUBCLÍNICA DE VENTRÍCULO DERECHO SISTÉMICO
MSc. Dra. Giselle Serrano Ricardoa, MSc. Dr. Adel E. González Morejóna, Dr. C. Luis E. Marcano Sanzb, MSc. Dr. Michel Cabrera Ortegac, MSc. Dr. Alfredo M. Naranjo Ugaldeb y MSc. Dr. Jesús F. Carballés Garcíad
______________
Departamentos de Ecocardiografíaa, de Cirugía Cardiovascularb, de Arritmias y Marcapasosc, y de Rehabilitación Cardiovasculard del Cardiocentro Pediátrico "William Soler". La Habana, Cuba.
Correspondencia: G. Serrano Ricardo. Cardiocentro Pediátrico "William Soler". Ave. 100 y Perla, Altahabana. Boyeros CP 10800. La Habana, Cuba. Correo electrónico: giselleserrano@infomed.sld.cu
Resumen
Introducción: La transposición de grandes arterias con corrección quirúrgica fisiológica predispone a la disfunción del ventrículo derecho sistémico. Se considera que los pacientes asintomáticos tienen una disfunción subclínica de este ventrículo. La ecocardiografía transtorácica se muestra sensible para evaluar la función ventricular derecha. Hasta la fecha, el tratamiento médico se inicia cuando el paciente comienza con síntomas sugestivos de disfunción ventricular. Objetivo: Estimar predictores ecocardiográficos de disfunción subclínica de ventrículo derecho sistémico. Método: Estudio observacional y prospectivo desde mayo 2011 hasta diciembre 2012. La muestra (n=65) se dividió en dos grupos: asintomáticos (n=33) y sintomáticos (n=32), según la ausencia o presencia de síntomas sugestivos de disfunción clínica del ventrículo derecho. Resultados: Los dos grupos resultaron homogéneos en relación con la edad y el tiempo de operación. En ambos se mostró hipertrofia de la pared anterior del ventrículo derecho, aunque menor en el grupo asintomático (p<0.001). Se evidenció disfunción sistólica subclínica en el grupo asintomático. No existieron diferencias en la función diastólica entre ambos grupos. Existieron correlaciones entre la recorrido sistólico del anillo lateral tricuspídeo y la fracción de eyección del ventrículo derecho, tanto en el grupo asintomático (r=0,68; IC 95 % 0,44 a 0,83; p<0.0001) como en el sintomático (r=0,77; IC 95 % 0,59 a 0,88; p<0.0001). Se identificaron predictores ecocardiográficos de disfunción subclínica de ventrículo derecho sistémico. Conclusiones: La edad, el grosor de la pared anterior del ventrículo derecho, el tiempo de operación, y los diámetros diastólico y sistólico del ventrículo derecho constituyen predictores ecocardiográficos de disfunción subclínica de ventrículo derecho sistémico, útiles para el inicio oportuno del tratamiento médico.
Palabras clave: Transposición de grandes arterias, Función ventricular, Ventrículo derecho sistémico, Ecocardiografía
Echocardiographic predictors of subclinical systemic right ventricular dysfunction
Abstract
Introduction: Transposition of the great arteries with physiological surgical correction predisposes to dysfunction of systemic right ventricle. It is believed that asymptomatic patients have a subclinical dysfunction of this ventricle. Transthoracic echocardiography is sensitive to assess right ventricular function. To date, medical treatment is started when the patient begins with symptoms suggestive of ventricular dysfunction. Objective: To estimate echocardiographic predictors of subclinical dysfunction of systemic right ventricle. Method: Observational prospective study from May 2011 to December 2012. The sample (n= 65) was divided into two groups: asymptomatic (n = 33) and symptomatic (n = 32), according to the absence or presence of clinical symptoms suggestive of right ventricular dysfunction. Results: The two groups were homogeneous in terms of age and surgical time. In both hypertrophy of the right ventricle anterior wall was showed, although lower in
the asymptomatic group (p < 0.001). Subclinical systolic dysfunction in the asymptomatic group was evident. There were no differences in diastolic function between the two groups. There were correlations between the tricuspid annular plane systolic excursion and the right ventricular ejection fraction, both in the asymptomatic (r = 0.68, CI 95 % 0.44 to 0.83, p < 0.0001) and symptomatic groups (r = 0.77, CI 95 % 0.59 to 0.88, p < 0.0001). Echocardiographic predictors of subclinical systemic right ventricular dysfunction were identified. Conclusions: Age, right ventricle anterior wall thickness, surgical time, and diastolic and systolic diameters of the right ventricle are echocardiographic predictors of subclinical systemic right ventricular dysfunction, useful for the timely initiation of medical treatment.
Key words: Transposition of the great arteries, Ventricular performance, Systemic right ventricle, Echocardiography
Introducción
La transposición de grandes arterias (TGA) es la cardiopatía congénita cianótica con concordancia aurículo-ventricular y discordancia ventrículo-arterial, más frecuente en el período neonatal1. Una de las opciones quirúrgicas es la corrección fisiológica, según las técnicas de Mustard2 o Senning3, cirugía auricular para reconducir los flujos venosos que provienen de las venas cava hacia el ventrículo izquierdo, de donde emerge la arteria pulmonar, mientras que el retorno proveniente de las venas pulmonares alcanza el ventrículo derecho (VD) que conecta con la arteria aorta; de modo que el VD sostiene la circulación sistémica. Esta situación se denomina VD sistémico.
La intervención quirúrgica corrige la hemodinámica, pero a largo plazo, predispone a padecer arritmias, obstrucción de túneles auriculares, insuficiencia valvular tricuspídea y disfunción de VD sistémico4-7. Aunque actualmente dicha técnica quirúrgica no constituye la primera elección, existen un número importante de pacientes operados que tienen síntomas, y otros que comienzan a tenerlos.
Es frecuente que el deterioro ventricular progrese, de manera solapada, antes de tener expresión clínica. Se considera que los pacientes asintomáticos tienen una disfunción subclínica de VD sistémico. Aunque existen limitaciones por la geometría compleja del VD y su posición retroesternal, la ecocardiografía transtorácica se muestra sensible para evaluar la función ventricular derecha en estos pacientes8-10. Hasta la fecha, el tratamiento médico se inicia cuando el paciente comienza con síntomas sugestivos de disfunción ventricular. Es probable que existan predictores ecocardiográficos de disfunción subclínica de VD sistémico, útiles para el inicio oportuno del tratamiento médico.
Método
Pacientes
Se realizó un estudio observacional y prospectivo desde mayo de 2011 hasta diciembre de 2012. Se estudiaron 65 pacientes con TGA y corrección quirúrgica fisiológica, integrantes del Programa Nacional de Rehabilitación Cardiovascular Pediátrica, a los cuales se les practicó estudio ecocardiográfico transtorácico en chequeo posquirúrgico anual, en el Departamento de Ecocardiografía del Cardiocentro Pediátrico "William Soler". Se solicitó la firma por escrito del consentimiento informado de todos los participantes en la investigación. La muestra se dividió en dos grupos: asintomáticos (n=33) y sintomáticos (n=32), según la ausencia o presencia de síntomas sugestivos de disfunción clínica de VD.
Ecocardiograma
A cada paciente se le realizó un ecocardiograma transtorácico, por un especialista experimentado (Nivel III de la Sociedad Americana de Ecocardiografía), con un equipo Aloka α-10 o Aloka 5500, transductores de 2,5 y 5,0 Mhz, y software incorporado para la realización de Doppler tisular espectral.
Con el paciente en decúbito supino o lateral izquierdo, bajo respiración pausada y en un medio ambiente adecuado, se realizaron las vistas convencionales (paraesternal, eje longitudinal y transversal), apicales de eje largo (cuatro, dos y cinco cámaras), y subcostales tradicionales y con sector invertido (ejes coronales y sagitales, y cortes oblicuos).
Variables
Se estudiaron las siguientes variables cuantitativas: edad, tiempo de operación, diámetros (de aurícula derecha, VD diastólico, VD sistólico), grosor de la pared anterior del VD, fracción de eyección del VD (FEVD), recorrido sistólico del anillo lateral tricuspídeo (TAPSE, por sus siglas en inglés), onda S del Doppler tisular, ondas Ea y Aa, así como la relación Ea/Aa (relación de ondas protodiastólica y telediastólica).
Procesamiento estadístico
Según la prueba de Kolmogorov-Smirnov, las variables que mostraron una distribución normal se resumieron como media y desviación estándar, mientras que aquellas con distribuciones no paramétricas se expresaron según mediana y rango intercuartílico. Para comparación de medias calculadas en ambos grupos de estudio se empleó la prueba paramétrica t de Student en las variables cuantitativas con distribuciones normales, y cuando las distribuciones no cumplieron esa condición, se utilizó la prueba no paramétrica U de Mann-Whitney con sustitución de las medias por las medianas. Siempre se tomó un intervalo de confianza de 95 %. Se construyeron dos modelos de correlación lineal simple, donde se identificó el coeficiente de correlación de Pearson (r) como expresión de la fuerza de asociación entre las dos variables cuantitativas: FEVD y TAPSE en ambos grupos de estudio. Para estimar los predictores ecocardiográficos de disfunción subclínica ventricular derecha se realizó una regresión logística, donde se identificaron el índice de probabilidad (OR - Odds Ratio, en su idioma original) y el estadígrafo Wald para cada variable. Para validar los resultados en términos de significación se utilizó un nivel de confianza de 95 %, y se consideró significativo todo valor de p ≤ 0.05 para el estadígrafo asociado a la prueba. Se utilizó el programa estadístico MedCalc versión 12.
Resultados
Ambos grupos de estudio resultaron homogéneos en relación con la edad y el tiempo de operación (Tabla 1). La edad mostró medias de 14,5 en el grupo asintomático y 17,2 en el sintomático; mientras que el tiempo de operación exhibió medias de 13,5 y 14,7 años en cada grupo, respectivamente.
Tabla 1. Edad y tiempo de operación (años).
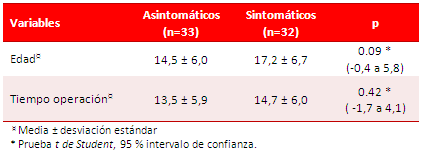
Los diámetros ventriculares y el grosor de la pared anterior de VD sistémico se muestran en la tabla 2. Se evidenció dilatación de las cavidades derechas: diámetros de aurícula derecha (p<0.001), VD diastólico (p<0.001) y VD sistólico (p<0.001) en el grupo sintomático (n=32); mientras que en el grupo asintomático (n=33) no existió una dilatación importante de dichas cavidades. En ambos grupos se demostró hipertrofia de la pared anterior de VD, aunque fue significativamente menor en el grupo asintomático (p<0.001).
Tabla 2. Diámetros ventriculares y grosor de pared anterior de VD sistémico (mm).
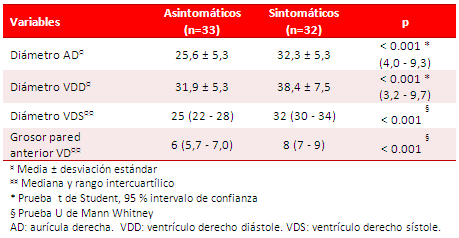
La tabla 3 presenta las variables ecocardiográficas para evaluar la función sistólica. El grupo sintomático presentó valores medios significativamente menores de FEVD (52,1 ± 8,7 %; p=0.025), de TAPSE (11,7 ± 3,4 mm; p=0.004) y de onda S del Doppler tisular 9,1 [(8,0 a 10,7 cm/s) (p=0.011)]. Aunque el grupo asintomático muestra valores medios mayores, estos constituyen parámetros de disfunción sistólica subclínica de VD sistémico.
Tabla 3. Función sistólica.
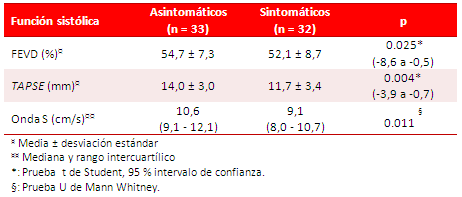
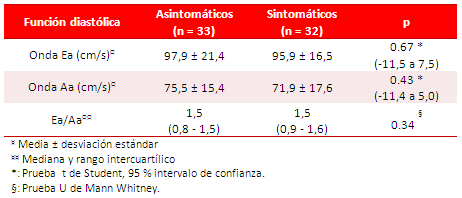
Ambos grupos presentaron valores ecocardiográficos de función diastólica similares (tabla 4), sin que existiera diferencia significativa entre cada uno de ellos: onda Ea [(p=0.67) (-11,5 a 7,5)], onda Aa [(p=0.43) (-11,4 a 5,0)] y relación Ea/Aa (p=0.34).
Tabla 4. Función diastólica.
La figura 1 exhibe la correlación lineal simple entre TAPSE y FEVD en el grupo sintomático con un coeficiente de correlación r = 0,77; con IC 95 % de 0,59 a 0,88 y p<0.0001; mientras que en el grupo asintomático (figura 2) el coeficiente de correlación fue r = 0,68; con IC 95 % de 0,44 a 0,83 y p<0.0001. Situación que demuestra la fuerza de asociación de ambas variables como evaluadoras de la función sistólica en los dos grupos de estudio.
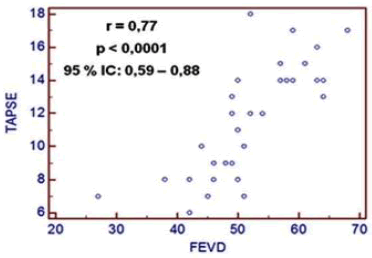
Figura 1. Correlación lineal simple, según FEVD y TAPSE en pacientes sintomáticos.
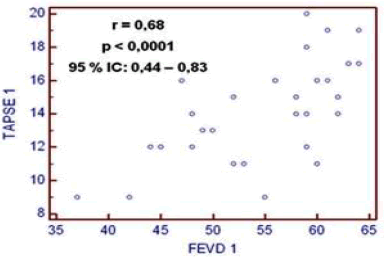
Figura 2. Correlación lineal simple, según FEVD y TAPSE en pacientes asintomáticos.
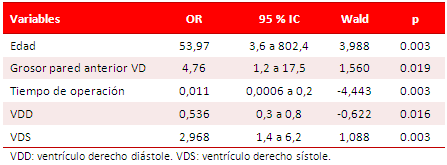
La tabla 5 presenta la regresión logística para demostrar la asociación de la disfunción subclínica de VD sistémico respecto a probables predictores ecocardiográficos de disfunción, donde se identificaron como significativas las siguientes variables: edad (OR: 53,97; IC 95 % 3,6 a 802,4; p = 0.003), grosor de pared anterior de VD (OR: 4,76; IC 95 % 1,2 a 17,5; p = 0.019), tiempo de operación (OR: 0,011;IC 95 % 0,0006 a 0,2; p = 0.003), diámetro diastólico de VD (OR: 0,536; IC 95 % 0,3 a 0,8; p = 0.016) y diámetro sistólico de VD (OR: 2,968; IC 95 % 1,4 a 6,2; p = 0.003).
Tabla 5. Regresión logística.
Discusión
Los pacientes con TGA y corrección quirúrgica fisiológica mantienen el ventrículo morfológicamente derecho en posición sistémica, situación que causa su disfunción a largo plazo. No se conoce con certeza la incidencia con la que se desarrolla fallo ventricular durante el seguimiento. Roos-Hesselink11 presentó cifras de 61 % a los 25 años, mientras que Moons12 mostró cifras menores (disfunción ventricular de 30 % de los enfermos), con supervivencia de hasta 85 % a los 32 años. Ebenroth13 informó, en un seguimiento a largo plazo de 45 pacientes, que 13 % de ellos fallecieron entre la segunda y tercera décadas de la vida. Solo se registra en la literatura una paciente de 49 años tratada con corrección quirúrgica fisiológica, en la etapa neonatal, con evolución favorable14.
La causa de la disfunción ventricular derecha postoperatoria es multifactorial. Se enuncian varios factores: a) falta de capacidad del VD para adaptarse a la función de bomba de la circulación sistémica; b) circulación coronaria mantenida por una arteria coronaria derecha que tiene que aportar todo el flujo sanguíneo al ventrículo sistémico; c) daño miocárdico producido por hipoxia intensa mantenida antes de la cirugía y d) daño perioperatorio provocado por insuficiente protección miocárdica15.
Se conoce que los síntomas de disfunción comienzan mientras más edad tengan los pacientes y el tiempo de operación sea mayor6,7. La disfunción ventricular sistémica asintomática persiste por prolongados períodos de tiempo antes que aparezcan los síntomas. Algunos pacientes presentan disfunción ventricular sistémica con una fracción de eyección disminuida o con dilatación de las cavidades cardíacas aún en ausencia de síntomas16.
En posición sistémica, el VD modifica la arquitectura de sus fibras musculares y se asemeja al patrón intercalado que se observa en el ventrículo izquierdo normal con orientación oblicua de fibras superficiales, longitudinales en el subendocardio y circunferenciales en el miocardio. El acortamiento de la pared libre es predominantemente circunferencial, en vez de longitudinal17,18. La pared anterior del VD suele tener un grosor entre 3 a 5 mm, pero en condiciones de sobrecarga de presión dicho espesor puede ser mayor, lo que establece la hipertrofia ventricular, aunque se desconoce si ello ayuda a normalizar la tensión de la pared o conduce a una disfunción contráctil. Está demostrada la hipertrofia en los VD sistémicos aún en la etapa subclínica. Estos cambios permiten al VD adaptarse, en gran medida y durante varias décadas, a la posición y la función sistémicas17,19.
La función ventricular derecha es una variable difícil de cuantificar debido a la compleja geometría del VD, es por ello que se considera la ecocardiografía transtorácica bidimensional un método certero, accesible y relativamente barato en la práctica clínica7.
La determinación de la FEVD es una herramienta importante, aunque es difícil definir la fracción de eyección normal en un ventrículo sistémico pues depende del método de determinación. Algunos autores consideran que la fracción estimada mayor de 55 % puede ser considerada normal (en ausencia de insuficiencia tricuspídea significativa). Como estimación cualitativa el método bidimensional posee mucho valor y está correlacionado con la fracción de eyección estimada por cateterismo cardíaco20. Se comprobaron valores menores de la FEVD en el grupo asintomático. De acuerdo a las medias de los valores obtenidos en el TAPSE y la onda S del Doppler tisular, se manifestó una disminución en el grupo sin síntomas, lo cual corresponde con lo informado por otros autores16,21,22.
Pocos estudios han demostrado la importancia pronóstica de la disfunción diastólica, ya que su estudio es complejo por su estrecha dependencia de la precarga y de los índices de llenado, lo cual justifica que no hayan existido diferencias entre ambos grupos de estudio21,23.
De acuerdo a los resultados, se identificó un grupo de probables predictores ecocardiográficos en la ocurrencia de disfunción subclínica de VD sistémico. Intervenir oportunamente durante esta etapa asintomática es crucial para modificar el pronóstico en términos de mejorar los síntomas por insuficiencia cardíaca, disminuir los días de hospitalización, reducir la mortalidad y mejorar la calidad de vida. Es importante el seguimiento periódico de los pacientes pues cuando se conocen los valores predictivos de disfunción subclínica se pueden trazar estrategias terapéuticas para preservar la función ventricular.
Conclusiones
La edad, el grosor de la pared anterior del VD, los diámetros de las cavidades cardíacas derechas y el tiempo de operación, son predictores ecocardiográficos de disfunción subclínica de VD sistémico.
Nota del editor
* Invasivo, este término viene del inglés invasive, cuya traducción directa es "invasivo/a". Siempre que se refiera a una técnica o procedimiento diagnóstico o terapéutico, es un anglicismo. La RAE acepta este
vocablo solamente como adjetivo derivado del verbo invadir. A su vez se refiere a la penetración en el
organismo sólo de agentes patógenos, por lo que no parece razonable aplicarlo a procedimientos diagnósticos o técnicas de tratamiento. La traducción más correcta, aunque no perfecta, es cruenta, que provoca efusión de sangre, también pueden ser agresivas, penetrantes. No obstante, CorSalud ha decidido aceptar invasivo/a debido a su alta frecuencia de uso y de que además, creemos no es razonable sustituir por otros términos que quizás no expresen con claridad la complejidad de este tipo de técnica quirúrgica.
Referencias bibliográficas
Salih C, Brizard C, Penny DJ, Anderson RH. Transposition. En: Anderson RH, Baker EJ, Penny DJ, Redington AN, Rigby ML, Wernovsky G, eds. Paediatric Cardiology 3ra. ed. London: Churchill Livingstone/Elsevier; 2010. p. 795-817.
Mustard WT. Successful two-stage correction of transposition of the great vessels. Surgery. 1964;55:469-72.
Senning A. Surgical correction of transposition of the great vessels. Surgery. 1959;45(6):966-80.
Baumgartner H, Bonhoeffer P, De Groot NM, de Haan F, Deanfield JE, Galie N, et al. Guía de práctica clínica de la ESC para el manejo de cardiopatías congénitas en el adulto. Rev Esp Cardiol. 2010;63(12):1484.e1-e59.
Schwerzmann M, Salehian O, Harris L, Siu SC, Williams WG, Webb GD, et al. Ventricular arrhythmias and sudden death in adults after a Mustard operation for transposition of the great arteries. Eur Heart J. 2009;30(15):1873-9.
Dos L, Teruel L, Ferreira IJ, Rodríguez-Larrea J, Miro L, Girona J, et al. Late outcome of Senning and Mustard procedures for correction of transposition of the great arteries. Heart. 2005;91(5):652-6.
Oechslin E, Jenni R. 40 years after the first atrial switch procedure in patients with transposition of the great arteries: long-term results in Toronto and Zurich. Thorac Cardiovasc Surg. 2000;48(4):233-7.
Sanz J, Fernández- Friera L, Moral S. Técnicas de imagen en la evaluación del corazón derecho y la circulación pulmonar. Rev Esp Cardiol. 2010;63(2):209-23.
Lai WW, Geva T, Shirali GS, Frommelt PC, Humes RA, Brook MM, et al. Guidelines and standards for performance of a pediatric echocardiogram: A report from the Task Force of the Pediatric Council of the American Society of Echocardiography. J Am Soc Echocardiogr. 2006;19(12):1413-30.
López L, Colan SD, Frommelt PC, Ensing GJ, Kendall K, Younoszai AK, et al. Recommendations for quantification methods during the performance of a pediatric echocardiogram: A report from the pediatric measurements writing group of the American Society of Echocardiography Pediatric and Congenital Heart Disease Council. J Am Soc Echocardiogr. 2010;23(5):465-95.
Roos-Hesselink JW, Meijboom FJ, Spitaels SEC, Van Domburg R, Van Rijen EHM, Utens EMWJ, et al. Decline in ventricular function and clinical condition after Mustard repair for transposition of the great arteries (a prospective study of 22-29 years). Eur Heart J. 2004;25(14):1264-70.
Moons P, Gewillig M, Sluysmans T, Verhaaren H, Viart P, Massin M, et al. Long-term outcome up to 30 years after the Mustard or Senning operation: a nationwide multicenter study in Belgium. Heart. 2004;90(3):307-13.
Ebenroth ES, Hurwitz RA. Long-term functional outcome of patients following the Mustard procedure: The next decade of follow-up. Congenit Heart Dis. 2007;2(4):235-41.
Greutmann M, Tobler D, Grewal J, Biaggi P, Oechslin E, Crean A, et al. A reminder from the past: A 49-year-old patient with transposition of the great arteries palliated with Dr. Thomas Baffes´ and Dr. William Mustard´s. Original operations. J Am Soc Echocardiogr. 2009;22(11):1310.e1-4.
Oliver JMR. Cardiopatías congénitas del adulto: residuos, secuelas y complicaciones de las cardiopatías congénitas operadas en la infancia. Rev Esp Cardiol. 2003;56(1):73-88.
Frogoudaki AA. Assessing the failing systemic right ventricle. Angiology. 2008;59(2 Suppl):S93-6.
Alonso-González R, Dimopoulos K, Ho SY, Oliver JM, Gatzoulis MA. Ventrículo derecho y cardiopatías congénitas en el adulto. Rev Esp Cardiol. 2010;63(9):1070-86.
Ho SY, Nihoyannopoulos P. Anatomy, echocardiography and normal right ventricular dimensions. Heart. 2006;92 (Suppl 1):12-3.
Greyson CR. Ventrículo derecho y circulación pulmonar: conceptos básicos. Rev Esp Cardiol. 2010;63(1):81-95.
Silverman NH, Snider R. The assessment of chamber size and ventricular function. En: Hachtel G, ed. Two-dimensional echocardiography in congenital heart disease. Norwalk Connecticut: Appleton-Century-Crofts; 1982. p. 247-64.
Winter MM, Bouma BJ, Hardziyenka M, de Bruin-Bon R, Tan HL, Konings TC. Echocardiographic determinants of the clinical condition in patients with a systemic right ventricle. Echocardiography. 2010;27(10):1247-55.
Miller D, Farah MG, Liner A, Fox K, Schluchter M, Hoit BD. The relation between quantitative right ventricular ejection fraction and indices of tricuspid annular motion and myocardial performance. J Am Soc Echocardiogr. 2004;17(5):443-7.
Caviedes IS, Polentzi UG. Fisiopatología del ventrículo derecho. Rev Chil Enf Respir. 2009;25:170-81.
Recibido: 17 de septiembre de 2013
Aceptado: 15 de octubre de 2013
Subir