CorSalud 2013 Ene-Mar;5(1):108-119
ARTÍCULO DE REVISIÓN
TAQUICARDIA POR REENTRADA DEL NODO AURÍCULO–VENTRICULAR
Lic. Raimundo Carmona Puertaa, Dr. Elibet Chávez Gonzáleza, Dra. Jéssica Mirella Mercedesb
______________
Servicio de Electrofisiología Cardíaca Clínica y Estimulación. Cardiocentro "Ernesto Che Guevara". Santa Clara, Villa Clara, Cuba.
Hospital Nacional San Rafael y Hospital Militar Central. San Salvador, El Salvador.
Correspondencia:R. Carmona Puerta. Calle B N° 15, entre Maceo y Manuel Ruiz. Reparto Villa Josefa. Santa Clara, CP 50200. Villa Clara, Cuba. Correo electrónico: raimundo@cardiovc.sld.cu
Resumen
La taquicardia por reentrada del nodo aurículo–ventricular representa una parte significativa de las taquiarritmias que los médicos asisten en los servicios de urgencias. Constituye la taquicardia paroxística más frecuente, y es característico que se presente sobre todo en mujeres entre la cuarta y la quinta década de la vida. El diagnóstico puede hacerse con alta fiabilidad mediante el electrocardiograma de superficie y algunos casos complejos o dudosos, mediante los estudios electrofisiológicos. Su tratamiento debe ser dirigido hacia la curación definitiva mediante la técnica de ablación endocavitaria, pero de acuerdo a su disponibilidad o las preferencias del paciente se puede indicar tratamiento farmacológico. En este artículo se resumen las técnicas diagnósticas, los tipos de taquicardia por reentrada intranodal y los principales aspectos del tratamiento.
Palabras clave: Taquicardia por Reentrada en el Nodo Atrioventricular, Ablación por Catéter, Tratamiento de Radiofrecuencia Pulsada, Electrocardiografía, Técnicas Electrofisiológicas Cardíacas
Abstract
Atrioventricular nodal reentrant tachycardia represents a significant part of tachyarrhythmias seen by attending physicians in emergency departments. It is the most common paroxysmal tachycardia, and it occurs primarily in women between their fourth and fifth decades of life. Diagnosis can be made with high reliability by surface electrocardiogram and complex or borderline cases by electrophysiological studies. Its treatment should be aimed towards definitive healing by endocardial ablation technique, but depending on availability or patient preferences drug treatment may be indicated. This article summarizes the diagnostic techniques, types of atrioventricular nodal reentrant tachycardia and major aspects of treatment.
Key words: Tachycardia, Atrioventricular Nodal Reentry, Catheter Ablation, Pulsed Radiofrequency Treatment, Electrocardiography, Cardiac Electrophysiologic Techniques
Introducción
En la historia del diagnóstico y tratamiento de las arritmias cardíacas es importante recordar varios hechos trascendentales que han contribuido al conocimiento actual en este campo, con respecto a ello podemos señalar que entre 1893 y 1907 se describe el sistema de conducción eléctrico cardíaco; a mediados del siglo XX se determinaron sus diferentes potenciales de acción y en 1968, fue posible el registro de la despolarización del haz de His mediante un catéter-electrodo intravascular1. Desde entonces la evolución de las técnicas de registro y estimulación para el estudio de las arritmias ha incrementado notablemente la comprensión de sus mecanismos, y ha permitido el desarrollo de nuevas modalidades terapéuticas basadas en la destrucción selectiva de áreas de miocardio, en las cuales se asientan partes esenciales de sustratos arritmogénicos1.
En este sentido, el desarrollo de las técnicas quirúrgicas para curar las arritmias comenzó en 1968 cuando el Dr. Hill Sealy satisfactoriamente, interrumpió una vía accesoria aurículo-ventricular (AV) localizada por mapeo epicárdico a la derecha del surco AV. Este suceso inició el desarrollo de técnicas quirúrgicas para el tratamiento del síndrome de Wolff-Parkinson-White, y subsecuentemente se fueron desarrollando técnicas innovadoras en el tratamiento de la taquicardia por reentrada intranodal (TRIN), taquicardia, flutter y fibrilación auriculares2.
En 1979 ocurrió un accidente que cambiaría la historia del tratamiento de las arritmias cardíacas, durante un estudio se produjo un bloqueo AV por un catéter endocavitario. Posteriormente, a inicios de la década de los ochenta se describió la técnica de fulguración con corriente directa y nació de este modo, la electrofisiología intervencionista. Se buscaron otras formas de energía y fue así como empezó a utilizarse la radiofrecuencia1. Técnica introducida en la clínica en 19823, y la electrocirugía la aplicación más típica dentro de ella.
Según Ardashev4, el primero en utilizar este tipo de energía fue Huang a finales de la década de los ochenta. Desde entonces su uso se ha extendido a nivel mundial para el tratamiento definitivo de la mayoría de taquiarritmias supraventriculares4, entre estas la TRIN5-7.
DIAGNÓSTICO
Epidemiología, interrogatorio y examen físico
Desde el punto de vista clínico la TRIN es más frecuente en mujeres2, con una media de edad de 40 ± 5 años y los síntomas pueden iniciarse a cualquier edad. Es menos frecuente su presentación en niños pequeños. Habitualmente se observa en pacientes sin cardiopatía estructural. Su presentación es esporádica pero existen raros casos familiares.
Los síntomas de presentación pueden ir desde palpitaciones, disnea, angina (el dolor precordial muchas veces no es típico), presíncope e incluso hasta el síncope. Algunos pacientes son simplemente interpretados como ansiosos, por ello puede demorarse mucho su diagnóstico, otros pueden cursar con manifestaciones de insuficiencia cardíaca franca. Las formas de presentación más graves se asocian a episodios muy rápidos, cardiopatía estructural previa y a pausas largas en el momento en que termina la arritmia, usualmente explicado por una depresión transitoria en la función del nodo sinusal. Los paroxismos pueden ser autolimitados, revertidos por el mismo paciente mediante maniobras vagales, o pueden requerir la asistencia de servicios de urgencias para su control. En nuestra experiencia hemos observado que casi la totalidad de los pacientes describen el inicio paroxístico de la taquicardia, pero la terminación para algunos es percibida como súbita y para otros, de enlentecimiento progresivo. En estudios electrofisiológicos y registros Holter se puede demostrar, que una buena cantidad de pacientes continúan con una taquicardia sinusal en los primeros minutos tras autolimitarse la TRIN. Esta es la base de que algunos de estos enfermos no puedan percibir con claridad la terminación paroxística de la taquicardia. Señalamos estos elementos porque el interrogatorio del paciente podría sugerirnos erróneamente un mecanismo de enfriamiento de foco, como el que es propio de las taquicardias automáticas, y orientarnos equívocamente a otros tipos de taquiarritmias. También tiene valor la sensación molesta de latidos fuertes en el cuello, que se visualizan en la inspección como ondas a cañón con una relación 1:1, respecto a los latidos arteriales percibidos en el pulso radial. Aunque también puede observarse en las taquicardias ortodrómicas por vías accesorias, menos manifiesta en este contexto, porque el tiempo de conducción ventrículo-auricular es más prolongado en estas taquicardias, lo que hace que se desarrollen presiones intraauriculares menores que las alcanzadas durante la TRIN. El mecanismo de este síntoma/signo es la contracción al unísono de las aurículas y los ventrículos, lo que produce un flujo de sangre reverso al interior de las venas yugulares durante la sístole auricular. La frecuencia cardíaca máxima que hemos observado en nuestros pacientes es de 290 latidos por minuto y la menor de 130, aunque estos valores no reflejan el comportamiento de la mayoría de los casos. Estos datos muestran que la frecuencia de la taquicardia no orienta el diagnóstico porque se solapa con una amplia variedad de posibilidades. Una minoría de pacientes refiere sentir deseos de miccionar durante las crisis de la arritmia, y de hecho se verifica un aumento de la diuresis. Esto parece deberse a la liberación de péptido natriurético atrial.
Diagnóstico electrocardiográfico
Se trata de una taquicardia regular con complejos QRS estrechos y ondas P retrógradas que guardan relación 1:1 con el QRS (Figura 1). El carácter retrógrado de las ondas P determina un intervalo RP<PR en la mayoría de los casos. Se producen pseudo ondas r´ (falsas fuerzas terminales del QRS) en derivaciones V1 y aVR, y pseudo ondas s (falsas fuerzas terminales del QRS) en derivaciones con complejos QRS predominantemente negativos. La onda P deberá ser obligatoriamente negativa en las derivaciones DII, DIII y aVF (manifestada como pseudo s o una onda P francamente definida), al reflejar la activación caudo-craneal de la aurícula derecha. En casi todas las esferas de la medicina existen excepciones, en este punto de la TRIN también. En la variante rápida-lenta aparece un intervalo RP>PR (brazo retrógrado del circuito con conducción muy lenta) y deberá efectuarse una diferenciación con la taquicardia sinusal, la auricular y la reciprocante permanente de la unión AV (taquicardia de Coummel). Debe destacarse que podrán aparecer intervalos RP<PR pero de una duración considerable, lo que nos lleva al diagnóstico erróneo de taquicardia ortodrómica, es por eso que intervalos RP entre 60-70 ms están en la zona de duda, y aquellos >80ms reducen casi totalmente la posibilidad de TRIN, pero no la excluyen totalmente. La existencia de tipos intermedios de TRIN nos obliga a estar preparados para encontrarnos, aunque sea rara vez, con intervalos RP diversos. En estos casos solo el estudio electrofisiológico (EEF) puede hacer la diferenciación. En un artículo ya clásico en nuestro medio, la Profesora Dra. Margarita Dorantes define que las presentaciones electrocardiográficas de la TRIN se resumen en: P superpuesta al QRS como fuerza terminal, RP < 60 ms, RP ≥ 60 ms, RP mayor que el PR y onda P por delante del QRS8.
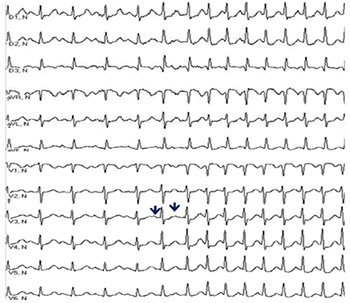
Figura 1. Electrocardiograma de 12 derivaciones obtenido de una mujer de 44 años de edad durante la inducción espontánea de un episodio de TRIN común, desencadenada por una pareja de extrasístoles auriculares (flechas).
Ocasionalmente no existe una relación 1:1 entre la onda P y el QRS, de ahí que ocurra una presentación electrocardiográfica poco habitual de la TRIN. Se produce una taquicardia lenta con un intervalo RP=PR (suponiendo que el médico que informa el electrocardiograma no se percate de la falsa r´ o de pseudo ondas s, y solo visualice la onda P que se inscribe en un punto intermedio entre dos complejos QRS de la taquicardia). Esto sucede por la ocurrencia de un bloqueo de la conducción anterógrado 2:1, a nivel del haz de His, con ausencia intermitente en la generación del complejo QRS. Otros grados mayores de bloqueo, como por ejemplo de alto grado o avanzado, serían teóricamente posibles de forma espontánea, lo que hace de la TRIN una arritmia de comportamiento irregular si dicho bloqueo se presenta de forma intermitente en breves períodos de tiempo. En nuestra experiencia nunca hemos encontrado esta suposición en una forma espontánea de presentación; pero la producción transitoria de este tipo de bloqueo en una paciente con TRIN común, durante un procedimiento de ablación, permitió comprobar que esto podría ser posible en pacientes con lesiones hisianas. Recordemos que el haz de His no forma parte obligatoria del circuito que determina la TRIN, por lo que su lesión espontánea, intencional o iatrogénica no detiene la taquicardia.
Ocasionalmente podrían ocurrir bloqueos retrógrados de la conducción hacia las aurículas, que produzcan ciertos grados de disociación aurículo-ventricular, pero algunos autores prestigiosos como Farré9 dudan la existencia de esta posibilidad, y argumentan que los escasos casos descritos probablemente hayan sido erróneamente etiquetados como TRIN. La existencia de esta forma de presentación apoyaría la confinación del circuito al nodo AV, cuando está confirmado por múltiples autores que en el circuito de la TRIN participan también fibras auriculares. Esto último determina la imposibilidad de disociación AV en este tipo de arritmia.
En múltiples ocasiones, mientras se monitoriza a estos pacientes durante un procedimiento de ablación, se ha visto una transformación espontánea de la TRIN en fibrilación auricular y viceversa, por lo que una historia referida de taquicardia con latidos en el cuello y una documentación de fibrilación auricular debe hacernos considerar tal posibilidad, sobre todo si es una mujer en la cuarta década de la vida.
Entre el 25 – 50 % de los pacientes pueden presentar un infradesnivel del segmento ST en presencia de arterias coronarias normales durante un episodio de TRIN, y puede documentarse una inversión transitoria de la onda T postaquicardia en el 40 % de los casos10.
Por último, es importante destacar que la TRIN podría manifestarse con QRS ancho si ocurriese: bloqueo de rama de fase 3, bloqueo de rama preexistente o presencia de vía accesoria con conducción anterógrada. En este último caso estaría formando parte del diagnóstico diferencial de las taquicardias regulares preexcitadas.
Diagnóstico electrofisiológico
El diagnóstico electrofisiológico de estas taquicardias viene efectuándose sistemáticamente desde los años setenta. Según Jackman et al.11, en 1973, Denes describe la presencia de doble vía atrioventricular nodal en el EEF de pacientes con TRIN, ahora se sabe qué curvas de períodos refractarios discontinuas pueden no estar presentes en todos los pacientes con esta taquicardia11. A partir de este concepto se reconoció clásicamente que el mecanismo de la TRIN era atribuido a la presencia de doble vía nodal: una rápida, con período refractario prolongado, y una lenta, con período refractario corto12.
En 1981, se dio un paso importante en el conocimiento de la reentrada en la vecindad del nodo AV, cuando, según Civera13, Sung y colaboradores demostraron que la conducción retrógrada a través de la vía lenta producía activación inicial en la parte posterior del tabique, próxima al ostium del seno coronario, mientras que la conducción retrógrada a través de la vía rápida produce la activación inicial en el vértice del triángulo de Koch en la zona distal del hisiograma13.
El mecanismo de esta arritmia, aunque no se conoce por completo, se encuentra razonablemente caracterizado. Así, hoy día se acepta que el nodo AV es una estructura más extensa de lo que se creía previamente, situada en el triángulo de Koch14, el cual está delimitado superior y anteriormente por el tendón de Todaro, posterior, por el seno coronario, e inferior, por la inserción septal de la válvula tricúspide; y en la base del triángulo, se encuentra, el ostium del seno coronario15.
Desde el punto de vista funcional, consta de al menos 2 conexiones con el miocardio auricular circundante. La primera de ellas, en una posición más craneal, que es conocida como vía nodal rápida y presenta una velocidad de conducción rápida y un período refractario prolongado, lo que condiciona que, a frecuencias auriculares lentas, el impulso cardíaco eléctrico se conduzca por ella en un tiempo breve, mientras que a frecuencias rápidas no es capaz de atravesar esta estructura. La segunda conexión, de localización más caudal y conocida como vía nodal lenta, presenta una velocidad de conducción lenta y un período refractario breve, lo que condiciona que, a frecuencias auriculares rápidas, cuando no hay conducción por la vía nodal rápida, el impulso eléctrico se conduce y alcanza los ventrículos en un tiempo más prolongado.
En algunos individuos es posible poner de manifiesto en el laboratorio de electrofisiología la presencia, bien diferenciada, de estas dos vías, mediante extra-estímulos eléctricos auriculares introducidos progresivamente, de forma cada vez más precoz, hasta que se bloquea la conducción por la vía nodal rápida, momento en el que se observa un incremento brusco y significativo (> 50 ms) en el intervalo de conducción aurículo-hisiano (intervalo AH). Este fenómeno se conoce como fisiología de doble vía nodal y el momento del incremento significativo, como salto del intervalo AH7,16,17.
La doble vía nodal constituye un modo frecuente de comportamiento de la conducción del nodo AV, al aparecer en un 10 a un 46 % de los individuos sometidos a un EEF, según las distintas series11,18,19. Su presencia no es universal en los pacientes con TRIN, ni en modo alguno explica que el paciente vaya a presentar este tipo de taquicardia de la unión AV9.
Estas características diferenciadas de las dos vías nodales condicionan, además, que ante una extrasístole auricular con acoplamiento corto, el impulso eléctrico pueda encontrar a la vía nodal rápida en su período refractario, y conducirse de forma muy lenta a través de la vía nodal lenta. La conducción lenta a través de esta última vía puede condicionar, a su vez, que la vía nodal rápida tenga tiempo de recuperar su capacidad de conducción en el momento en que el impulso alcanza el extremo distal de la vía nodal lenta, en su inserción común con la vía nodal rápida sobre el haz de His. En esta situación, el impulso se conducirá, además, de anterógradamente, a través del haz de His hacia los ventrículos, de manera retrógrada a través de la vía nodal rápida hacia las aurículas, desde donde puede reentrar en la vía nodal lenta, perpetuar esta secuencia y dar lugar a la denominada TRIN de tipo común o lenta-rápida (Figura 2), la cual puede ser inducida tanto por extrasístoles auriculares como ventriculares, esta secuencia también se puede producir en sentido inverso, lo que da lugar a la denominada TRIN no común o rápida-lenta, que también se puede inducir de ambas formas con alta posibilidad desde el ventrículo, y con una incidencia aproximada 10 veces menor que el tipo común7.
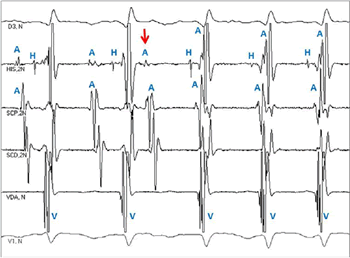
Figura 2. EEF del caso anterior. Los dos primeros latidos son sinusales. La flecha indica a una extrasístole auricular, la cual induce una prolongación considerable (más de 50 ms) del intervalo AH (compárese con los dos intervalos AH previos). La ocurrencia de este fenómeno indica doble fisiología nodal. Posterior a esto queda establecida una TRIN común, apréciese que los electrogramas auriculares coinciden con el complejo QRS en derivaciones DIII y V1 (primer y último canal de registro). His: registro del hisiograma, SCP y SCD: registros desde el seno coronario proximal y distal, respectivamente, VDA: punta del ventrículo derecho. A: electrogramas auriculares, V: electrogramas ventriculares, H: despolarización del haz de His.
El diagnóstico electrofisiológico de la TRIN se realiza tomando en cuenta13:
El inicio y el cese de la taquicardia por estimulación programada del corazón: con la estimulación programada puede demostrarse, en la mayoría de los casos, la presencia de una conducción AV o VA (ventrículo-auricular) discontinua; sin embargo, éste no es un criterio necesario ni suficiente para el diagnóstico de reentrada nodal.
Una secuencia de activación auricular durante la taquicardia compatible con un origen cercano al nodo AV (en el tabique interauricular, entre las zonas de registro del hisiograma y el ostium del seno coronario). La primera activación auricular registrada por el catéter de His sugiere TRIN común y la primera activación en seno coronario proximal, sugiere el tipo no común.
La ausencia de criterios positivos que indiquen la utilización de una vía accesoria AV septal13.
TIPOS DE TRIN
Lockwood et al.20 en su experiencia con 734 pacientes remitidos a su servicio para ablación de la TRIN, hallaron que 515 casos (77 %) tenían la forma lenta-rápida, 80 pacientes (11 %) la variante lenta-lenta, mientras que 89 (12 %) presentaron la forma rápida-lenta20. La variante lenta-rápida comprende tres subtipos electro-anatómicos bien definidos con consecuencias prácticas en la ablación de la vía lenta del circuito. En la primera forma (la más frecuente) la vía lenta es una extensión derecha inferior, otra variante tiene extensión inferior izquierda, y existe un modo de presentación más raro (2 %), donde la vía lenta anterógrada proviene de una región ubicada en el anillo mitral póstero-inferior, esta localización en la región posterior del anillo mitral constituye un desafío terapéutico porque la arritmia se presenta simulando una taquicardia ortodrómica, que emplea una vía accesoria posterior izquierda. Obsérvense las figuras 3 y 4 para una visión ilustrada de esta explicación.
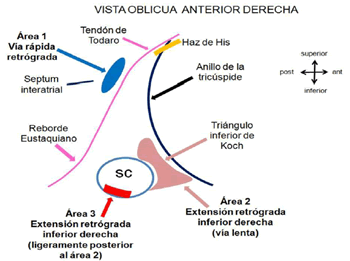
Figura 3. Representación esquemática de los sitios de activación auricular más precoces durante impulsos retroconducidos por la vía rápida y lenta. Vista oblicua anterior derecha. SC: seno coronario. Tomada de: Lockwood D, et al. Arrythmias and Electrophysiology 2008. p. 615-4620. Modificada por los autores.
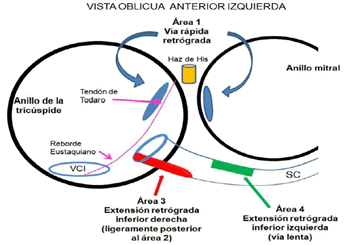
Figura 4. Representación esquemática de los sitios de activación auricular más precoces durante impulsos retroconducidos por la vía rápida y lenta. Vista oblicua anterior izquierda. VCI: vena cava inferior, SC: seno coronario. Tomada de: Lockwood D, et al. Arrythmias and Electrophysiology 2008. p. 615-4620. Modificada por los autores.
En el caso presentado por Montes et al.21 se observa que la primera activación auricular retrógrada ocurría en los polos 5 y 6 de un catéter decapolar situado en el seno coronario. El ingreso al nodo AV desde estas extrañas vías ocurre de la forma siguiente: 1) a través de la fosa oval y del ingreso anterior, 2) por la musculatura del seno coronario y del ingreso posterior, y 3) directamente a través del anillo mitral22. En este último ejemplo la ablación se consigue desde el lado izquierdo del corazón y puede simular fácilmente una vía accesoria oculta izquierda. La ocurrencia de un fenómeno 2 para 1 permite sospechar esta subvariante de TRIN lenta-rápida. Ello se refiere a que el haz de His es despolarizado doblemente, primero por un frente de onda proveniente de la vía rápida y unos milisegundos más tarde, por otro estímulo procedente de la vía lenta, que discurre desde la aurícula izquierda23.
Lenta – rápida
En esta forma de taquicardia, la activación atrial aparece antes, durante o justo después del complejo QRS manteniendo una relación AH/HA (Aurícula-His/His-Aurícula) > 1. En particular, un AH/HA > 3 y un intervalo VA medido desde el inicio de la activación ventricular en el electrocardiograma de superficie a la deflexión más precoz de la activación atrial en el electrograma del His < 60 ms, o un intervalo VA medido desde el atrio derecho < 95 ms, son diagnósticos de TRIN tipo lenta-rápida23. En 1985 Ross y colaboradores24 clasificaron esta variedad de taquicardia lenta-rápida en dos subtipos: el tipo A o anterior, es el más frecuente y se caracteriza por presentar, durante la taquicardia intervalos VA y HA cortos, (VA iguales o menores a 40 ms)24, inscripción del auriculograma dentro del complejo QRS y activación auricular más precoz en la derivación del hisiograma. En el tipo B o posterior, mucho más raro, la activación auricular retrógrada durante la taquicardia, se localiza en el tabique posterior, en la zona del ostium del seno coronario. Los intervalos VA y HA durante la taquicardia pueden variar aunque suelen ser más largos que en el tipo anterior (VA mayor de 40 ms, siendo la relación AH/HA < 1)13.
Estudios posteriores13,15,24, basados en el análisis de casos con formas múltiples de reentrada intranodal, sugieren que los tipos anterior y posterior de la taquicardia lenta-rápida utilizan diferentes circuitos y no representan meramente, una inversión del circuito habitual (vías α y β), sino una forma de reentrada distinta. Así las taquicardias tipo B utilizan de forma anterógrada la vía lenta (Α), y de forma retrógrada, una vía de salida posterior y tiempos de conducción intermedios (γ). Algunos de los casos de taquicardias, clasificados como del tipo posterior, muestran intervalos AH y HA largos, con relaciones AH/HA iguales o superiores a 113.
Rápida – Lenta
En esta forma de taquicardia (5-10 % de todos los casos de TRIN), el electrograma auricular retrógrado está después de la activación ventricular con una relación AH/HA < 1, lo que indica que la conducción retrógrada es más lenta que la conducción anterógrada. El intervalo VA, medido desde el inicio de la activación ventricular en el electrograma de superficie, hasta la deflexión más precoz de la activación atrial en el electrograma de His, es > 60 ms; y en la aurícula derecha alta > 100 ms. Desde el punto de vista electrocardiográfico esto produce una taquicardia con un intervalo RP mayor que el PR. En la mayoría de los casos de taquicardia rápida-lenta, el lugar de activación atrial precoz es posterior al nodo AV cerca del orificio del seno coronario. Sin embargo, se han descrito formas anteriores y medias de la TRIN rápida–lenta23,25.
Lenta – Lenta
En esta forma, la relación AH/HA es mayor de 1, pero el intervalo VA es > 60 ms, lo que sugiere que las dos vías lentas son utilizadas, ambas para la activación anterógrada y retrógrada. Usualmente, pero no siempre, la activación atrial más precoz es en el septum posterior (ostium del seno coronario). En la taquicardia posterior el tiempo de conducción VA puede ser prolongado, en un rango que va desde 78 a 168 ms. La relación aurícula-His/His-aurícula, sin embargo, permanece mayor que 1. Esto demuestra que casos informados como formas posteriores de la TRIN lenta-rápida representan actualmente la forma lenta-lenta descrita por Baerman, según Jackman et al.11.
Rápida – Rápida
Más recientemente, Wu et al.19 han demostrado la existencia de casos de TRIN que no se ajustan a los tipos descritos previamente. Esta taquicardia, denominada rápida-rápida, se caracteriza por una frecuencia más alta, intervalos AH y HA relativamente cortos, una relación AH/HA de alrededor de 1 y una activación auricular más precoz, próxima al ostium del seno coronario13,23,25.
Sobre el origen del circuito
Algunos autores26 plantean que la TRIN es el resultado de propiedades funcionales de anisotropía del tejido dentro del triángulo de Koch, más que dos o más vías anatómicas, es decir, que esta arritmia es el resultado de una disociación funcional longitudinal dentro del nodo AV. Sin embargo, estudios más recientes20-23 sugieren que la vía rápida y lenta involucradas en el circuito de reentrada de la TRIN representan la conducción sobre diferentes conexiones atrio-nodales, en vez de ser producto de una disociación funcional longitudinal dentro del nodo AV compacto. Estas observaciones incluyen:
Diferencias en el lugar de la activación atrial más precoz durante la conducción por la vía lenta o rápida, originalmente descritas por Sung y colaboradores.
Tratamiento eléctrico de la taquicardia por extraestímulos atriales aplicados fuera del nodo AV compacto en la parte inferior del triángulo de Koch o en el seno coronario.
Registros extracelulares y mapeo óptico de la conducción AV en perros y conejos.
Eliminación selectiva de la conducción de la vía rápida o lenta por ablación en el atrio lejano del nodo AV compacto.
TRATAMIENTO FARMACOLÓGICO Y NO FARMACOLÓGICO
TRATAMIENTO DE LA CRISIS
Maniobras vagales
Se aplican en el contexto agudo de una crisis de taquicardia porque producen hipertono vagal en el nodo AV, lo que deteriora las propiedades electrofisiológicas sustentadoras del movimiento circular del impulso.
Se recomienda como primera opción en pacientes con TRIN, hemodinámicamente estables, y como una medida ambulatoria que se le explica al paciente. Dichas maniobras son: compresión de globos oculares que induzcan cierto grado de dolor (muchos no la emplean por el peligro de ocasionar lesiones oculares), lavarse la cara con agua helada, maniobra de Valsalva (la más empleada) y maniobra de Müller (igual que la de Valsalva pero inverso, es decir, inspiración con glotis cerrada). También puede realizarse masaje del seno carotídeo mediante una compresión de 5-10 segundos, al tener en cuenta que la inervación vagal del corazón es lateralizada, por lo que el masaje sobre el seno carotídeo izquierdo ejerce mayor influencia sobre el nodo AV, dentro del cual está el sustrato que estamos tratando. El seno derecho guarda mayor relación con el nodo sinusal. No obstante, desde ambos lados, puede lograrse la terminación de la taquicardia porque existen fibras cruzadas en mayor o menor grado.
Hemos visto espectaculares casos donde, de tan solo tocar los globos oculares la arritmia termina; sin embargo, en la inmensa mayoría de los casos que llegan al cuerpo de guardia o en otros escenarios no se consigue terminar el episodio con estas medidas y se necesita emplear otras estrategias.
Tratamiento farmacológico
Se empleará si no hay deterioro hemodinámico ni contraindicaciones al fármaco que se va a emplear. Las opciones más utilizadas son:
Adenosina: bolo intravenoso de 6-12 mg. Contraindicaciones: asmáticos (broncoespasmo) y enfermedad coronaria.
Verapamilo: la administración de 10 mg intravenoso en 5 minutos posee una eficacia similar a la adenosina. En nuestra experiencia hemos logrado interrumpir la taquicardia con solo 2,5 mg, combinado o no con maniobra de Valsalva en una cantidad nada despreciable de pacientes. Esto reduce los efectos indeseables en dependencia de la dosis empleada. Contraindicaciones: hipotensión y mala función ventricular.
Otros fármacos durante la crisis: diltiazem, esmolol, metoprolol, digoxina y amiodarona.
Cardioversión eléctrica
La cardioversión eléctrica constituye la opción universal ante cualquier taquiarritmia con deterioro hemodinámico. Se induce sedación con propofol o midazolam. Casi todos los casos son efectivos con bajas cargas, de ahí que sea raro tener que emplear dosis superiores a 100 J en modalidad bifásica. Consideramos que es razonable su empleo si el médico comienza a notar rebeldía farmacológica del episodio aunque no hayan signos de deterioro hemodinámico. Esta recomendación se basa en que hemos visto emplear disímiles opciones farmacológicas en un mismo paciente, y cuando finalmente, se opta por la cardioversión, se han producido enormes pausas y asistolia que perturban el adecuado tratamiento del caso. Dichas pausas favorecidas por el empleo indiscriminado de los antiarrítmicos parenterales.
TRATAMIENTO DE MANTENIMIENTO
Se podrán emplear depresores de la conducción del nodo AV por vía oral, como: β-bloqueantes, verapamilo, diltiazem, y fármacos de la clase IC con acción sobre tejidos de conducción rápida (propafenona y flecainida). Estos fármacos, clase IC, parecen ejercer su efecto sobre la vía rápida del nodo AV o quizás actúan sobre las fibras de transición. Particularmente las hemos visto muy efectivas después de fallar los medicamentos clásicamente empleados. La digoxina, aunque podría constituir una opción, cada vez se usa menos para esta indicación. Excepcionalmente podrá emplearse amiodarona en casos rebeldes a las otras propuestas, en pacientes que rechazan la ablación endocavitaria o esta no es posible.
Maniobras vagales sin fármacos de mantenimiento: Son útiles en pacientes con TRIN altamente respondedora a estas maniobras y con comportamiento no recurrente de la taquicardia.
Píldora en el bolsillo: Está formalmente indicada como una opción en ciertos pacientes con fibrilación auricular, pero no ampliamente aceptado en la TRIN. No obstante, Almendral et al.10 la mencionan en su reciente revisión y reconocen que, por su efecto demorado (1-3 horas), podría ser poco práctico su uso ya que los efectos de la taquicardia pudieran ser insoportables si tuviera que esperarse tanto tiempo para controlarla.
Ablación por radiofrecuencia
La ablación con esta técnica se describió por primera vez en 1989, año en el que Haissaguerre27 publica el resultado de la ablación en 21 pacientes con TRIN. En el mismo año, según Civera et al.13, Sanjuán y colaboradores publicaron los resultados de la ablación con radiofrecuencia en cuatro pacientes. Inicialmente se abordaba la vía nodal rápida, pero esto producía con frecuencia prolongación del intervalo PR basal y una incidencia de bloqueo AV completo iatrogénico significativo. La prolongación del intervalo PR podía ser tan exagerada que algunos pacientes desarrollaban un síndrome de pseudomarcapasos.
En este sentido se han realizado múltiples estudios, los cuales comparan la ablación de la vía lenta o la rápida. El estudio MERFS (Multicenter European Radiofrequency Survey) analizó retrospectivamente la incidencia de complicaciones relacionadas con el procedimiento en 4.463 pacientes, quienes habían recibido ablación por radiofrecuencia en 69 instituciones europeas entre el año 1987 y 1992. En este estudio se evidenció que el bloqueo AV completo fue significativamente más frecuente en pacientes que habían recibido ablación de la vía rápida28.
Según Otomo29 y Marine30, en 1990, en una comunicación al congreso de la NASPE (North American Society of Pacing and Electrophysiology), Román y colaboradores demostraron que la ablación con radiofrecuencia del tabique interauricular posterior, próximo al ostium del seno coronario, era capaz de eliminar la conducción por la vía lenta e inhibir el desencadenamiento de la taquicardia, sin provocar ningún grado de bloqueo AV. Este hecho despertó un gran interés y se desarrollaron varias técnicas con este fin en distintos laboratorios. En el momento actual, la ablación dirigida a la vía nodal lenta constituye el procedimiento de elección para el tratamiento definitivo de esta taquicardia29,30.
Desde su comienzo se han realizado diversos estudios que han expuestos los resultados de esta técnica en múltiples centros31,32, todos con porcentajes de éxito mayores al 90 %. Tolpilski et al.33 exponen en su estudio de 14 años de experiencia en la ablación de esta taquicardia, un porcentaje de éxito mayor del 97 %, con un número de complicaciones menor al 5 %.
Datos del primer Registro Argentino de Ablación por Catéter34 revelan un éxito de 98,7 % en el primer intento de ablación de este sustrato, después de haber llevado a cabo esta terapia en 237 pacientes. Las complicaciones fueron mínimas: un paciente con bloqueo AV completo y otro que presentó un hematoma en el sitio de punción, lo que representó un 0,8 % de complicaciones. En España, según datos del X Informe Oficial de la Sección de Electrofisiología y Arritmias de la Sociedad Española de Arritmias y Marcapasos35, la TRIN representó el 27 % (2.321 procedimientos) de todos los sustratos abordados en el año 2010, que fueron 8.762. El porcentaje de éxito fue de 98,4 % aunque es significativo destacar que en 34 centros se alcanzó el éxito en el 100 % de las intervenciones de ablación. Se reportaron 8 casos con complicaciones (0,34 %), siendo el bloqueo AV completo, que requirió implante de marcapasos definitivo, la más frecuente (3 casos, 0,13 %); junto a tres pacientes que presentaron complicaciones relacionadas con el acceso vascular. Además se informó un caso con accidente cerebrovascular y otro con tromboembolismo pulmonar.
Este procedimiento se realiza además en la población pediátrica36-38 y en la geriátrica39, con muy buenos resultados.
Recomendaciones de ablación por radiofrecuencia en la TRIN40-44
Recientemente la Sociedad Colombiana de Cardiología publicó sus Guías de Electrofisiología Cardiovascular41,42, tras evaluar toda la información disponible al respecto procedente de las guías prácticas más reconocidas.
Clase I
El EEF con mapeo y ablación se indica en pacientes con TRIN sostenida y sintomática, que es resistente al tratamiento farmacológico o que no toleran la medicación antiarrítmica, no desean tratamiento farmacológico a largo plazo o tienen una profesión que se considera de alto riesgo (pilotos comerciales) (nivel de evidencia B).
Clase II
El EEF con mapeo y ablación es razonable en pacientes con TRIN identificada en un EEF o en la ablación de otra arritmia cardíaca.
El EEF con mapeo y ablación es razonable en pacientes con sospecha clínica de TRIN en quienes, durante un EEF, se encuentra doble vía nodal y ecos auriculares, pero sin TRIN.
Las guías colombianas no reconocen situaciones que conlleven a una indicación de clase III en el contexto de esta arritmia42. Sin embargo, las de la ACC/AHA43 sí prevén tal situación y la exponemos a continuación:
Clase III
Pacientes con TRIN bien toleradas, que responden a los fármacos antiarrítmicos y que el paciente prefiere a la ablación.
El hallazgo de fisiología de doble vía nodal (con o sin complejos de eco) durante el EEF de pacientes en quienes no se sospecha TRIN clínica.
También se ha empleado como técnica de abordaje por catéter la crioablación. Esta es una opción considerada más segura que la radiofrecuencia porque aunque induce bloqueo AV durante las aplicaciones hasta en el 6 % de los casos, estos tienden a desaparecer siempre que se detienen las aplicaciones40,43.
Referencias bibliográficas
Araya Gómez V. Electrofisiología intervencionista: Procedimientos diagnósticos y terapéuticos en arritmias cardiacas. Rev Costarric Cardiol [Internet]. 1999 [citado 27 Oct 2012];1(1):[aprox. 4 p.]. Disponible en: http://www.scielo.sa.cr/scielo.php?script=sci_arttext&pid=S1409–41421999000100004&lng=es
Josephson ME. Supraventricular tachycardias. In: Josephson M, editor. Clinical cardiac electrophysiology techniques and interpretations. 3rd ed. Philadelphia: Lippincott Williams and Wilkins; 2001. p. 103–51.
Iturralde Torres P, Colín Lizalde L, Guevara Valdivia M, Rodríquiz Chávez L. Experiencia en 1,500 pacientes sometidos a ablacion con radiofrecuencia en el tratamiento de las taquicardias. Arch Inst Cardiol Mex. 2000;70:349–366.
Ardashev AV, Zheliakov EG, Shavarov AA. Remote clinical results of treatment of atrioventricular nodal reciprocated with the use of novel and traditional methods of radiofrequency catheter ablation of slow part pathway of atrioventricular junction. Kardiologiia. 2010;50(3):56–64.
Femenia FJ, Peñafort F, Florentino C, Arrieta M, Gutiérrez A. Taquicardia por reentrada nodal: ablación por radiofrecuencia utilizando una técnica simplificada. Resultados y seguimiento a largo plazo. Rev Fed Arg Cardiol. 2008;37(2):148–53.
Azara D, Ruffa H, Mazo G, Rocchinotti M, Pelliza M. Experiencia con la ablación de corta duración de la vía lenta en paciente con taquicardias por reentrada intranodal.Rev Electro y Arritmias 2008;1(2):48–53.
Merino JL. Ablación de la taquicardia intranodal: cuando la fisiología cuenta en la era de la anatomía. Rev Esp Cardiol 2007 60(1): 7–9.
Dorantes M, Castro J, Rodríguez I, Zayas R, Dorticós F. Taquicardias ortodrómicas e intranodales. Equívocos diagnósticos y ablación. Rev Cubana Cardiol Cir Cardiovasc. 1999;13(1):46–52. Disponible en: http://www.bvs.sld.cu/revistas/car/vol13_1_99/car08199.pdf
Farré J, Wellens HJ, Rubio JM, Benezet J. Supraventricular Tachycardia. In: Camm AJ, Lüscher TF, Serruys PW, eds. The ESC Textbook of Cardiovascular Medicine. Oxford: Oxford University Press, 2009; p. 1013–88.
Almendral J, Castellanos E, Ortiz M. Taquicardias paroxisticas supraventriculares y sindromes de preexcitacion. Rev Esp Cardiol. 2012;65(5):456–69.
Jackman WM, Beckman KJ, McClelland JH, Wang X, Friday KJ, Roman CA, et al. Treatment of supraventricular tachycardia due to atrioventricular nodal reentry, by radiofrequency catheter ablation of slow–pathway conduction. N Engl J Med. 1992;327(5):313–8.
Josephson ME, Kastor JA. Paroxysmal supraventricular tachycardia: is the atrium a necessary link? Circulation.1976;54(3):430–5.
García Civera R, Ruiz Granell R, Morell Cabedo S, Sanjuán Máñez R, León JM, Botella Solana S, et al. Taquicarida por reentrada intranodal. En: Electrofisiología cardíaca clínica y ablación. España: McGraw–Hill Interamericana; 1999.
Lee PC, Chen SA, Hwang B. Atrioventricular node anatomy and physiology: implications for ablation of atrioventricular nodal reentrant tachycardia. Curr Opin Cardiol. 2009;24(2):105–12.
Eksik A, Akyol A, Norgaz T, Erdinler I. Influence of atrioventricular nodal reentrant tachycardia ablation on right to left Inter–atrial conduction. Indian Pacing Electrophysiol J. 2005;5(4):279–88.
Abedin Z, Conner R, editors. AV node reentry tachycardias. In: Abedin Z, Conner R. Esencial cardiac electrophysiology. Texas: Blackwell Futura; 2007. p. 94–103.
Katritsis DG. Left septal slow pathway ablation for atrioventricular nodal reentrant tachycardia. Europace. 2010;12(7):1042–3.
Wu D, Denes P, Amat–Y–León F, Dhingra R, Wyndham C, Bauernfeind R, et al. Clinical, electrocardiographic and electrophysiologic observations in patients with paroxysmal supraventicular tachycardia. Am J Cardiol. 1978;41(6):1045–51.
Wu D, Yeh SJ, Wang CC, Wen MS, Lin FC. A simple technique for selective radiofrequency ablation of the slow pathway in atrioventricular node reentrant tachycardia. J Am Coll Cardiol. 1993;21(7):1612–21.
Lockwood D, Nakagawa H, Jackman WM. Electrophysiologic characteristics of atrioventricular nodal reentrant tachycardia: Implications for reentrant circuits. In: Zipes DP, editor. Arrythmias and Electrophysiology. 2008. p. 615–46.
Montes JP, Barja LD, Pellegrino GMM, Ortega DF, Logarzo E, Mangani M. Reentrada intranodal atípica: doble respuesta ventricular asociada con activación retrograda izquierda. Rev Fed Arg Cardiol. 2009;38(4):211–15.
Azara D, Ruffa H, Pelliza M, Rochinotti M, Reynoso M. Taquicardia por reentrada nodal "lenta–rápida" izquierda. ¿Dónde ablacionar? Electrofisiología y Arritmias [Internet]. 2010 [citado 2 Abr 2012];(1):[aprox. 3 p.]. Disponible en: http://www.electrofisiologia.org.ar/joomla/index.php/menuanteriores/volumen4/numero–1/111–taquicardia–reentrada–nodal
Katritsis GD, Camm JA. Classification and differential diagnosis of atrioventricular nodal re–entrant tachycardia. Europace. 2006;8(1):22–36.
Ross DL, Johnson DC, Denniss AR, Cooper MJ, Richards DA, Uther JB. Curative surgery for atrioventricular junctional ("AV nodal") reentrant tachycardia. J Am Coll Cardiol. 1985;6(6):1383–92.
Heidbuchel H, Jackman WM. Characterization of subforms of AV nodal reentrant tachycardia Europace. 2004;6(4):316–29.
Kwaku KF, Josephson ME. Typical AVNRT–an update on mechannisms and therapy. Card Electrophysiol Rev. 2002;6(4):414–21.
Haissaguerre M, Warin JF, Lemetayer P, Saoudi N, Guillem JP, Blanchot P. Closed–chest ablation of retrograde conduction in patients with atrioventricular nodal reentrant tachycardia. N Engl J Med. 1989;320(7):426–33.
Hindricks G. Incidence of complete atrioventricular block following attempted radiofrequency catheter modification of the atrioventricular node in 880 patients. Results of the Multicenter European Radiofrequency Survey (MERFS) The Working Group on Arrhythmias of the European Society of Cardiology. Eur Heart J. 1996;17(1):82–8.
Otomo K, Okamura H, Noda T, Satomi K, Shimizu W, Suyama K, et al. "Left variant" atypical atrioventricular nodal reentrant tachycardia: Electrophysiological characteristics and effect of slow pathway ablation within coronary sinus. J Cardiovasc Electrophysiol. 2006;17(11):1177–883.
Marine JE. Catheter ablation therapy for supraventricular arrhythmias. JAMA. 2007;298(23):2768–78.
Calkins H, Yong P, Miller JM, Olshansky B, Carlson M, Saul JP, et al. Catheter ablation of accessory pathways, atrioventricular nodal reentrant tachycardia, and the atrioventricular junction: Final results of a prospective, multicenter clinical trial circulation. 1999;99(2):262–70.
Yu S, Zeng Q, Zhang J, Chen Z, Li J, Lei M. Clinical study on the treatment of 325 cases of atrioventricular node reentrant tachycardia by radiofrequency catheter ablation. J Tongji Med Univ. 2001; 21(1):23–5.
Tolpilski I, Rogowski O, Glick A, Viskin S, Eldar M, Belhassen B. Radiofrequency ablation of atrioventricular nodal reentry tachycardia: A 14 year experience with 901 atients at the Tel Aviv Sourasky Medical Center. Isr Med Assoc J. 2006;8(7):455–8.
Gant López J, Labadet C, González JL, Retyk E, Cáceres Monié C, Garro H. Primer registro argentino de ablación con catéter. Rev Arg Cardiol. 2011;79(2):117–24.
Macías Gallego A, Díaz–Infante E, García–Bolao I. Registro español de ablación con catéter. X Informe Oficial de la sección de Electrofisiología y Arritmias de la Sociedad Española de Arritmias y Marcapasos (2010). Rev Esp Cardiol. 2011;64(12):1147–53.
Hwang HK, Wolff GS, Sun FJ, Young ML. The most common site of success and its predictors in radiofrequency catheter ablation of the slow atrioventricular nodal pathway in children. Pacing Clin Electrophysiol. 2008;31(10):1300–6.
Friedman RA, Walsh EP, Silka MJ, Calkins H, Stevenson WG, Rhodes LA, et al. NASPE Expert Consensus Conference: Radiofrequency catheter ablation in children with and without congenital heart disease. Report of the writing committee. North American Society of Pacing and Electrophysiology. Pacing Clin Electrophysiol. 2002;25(6):1000–17.
Vida VL, Calvimontes GS, Macs MO, Aparicio P, Barnoya J, Castaneda AR. Radiofrequency catheter ablation of supraventricular tachycardia in children and adolescents : feasibility and cost–effectiveness in a low–income country. Pediatr Cardiol. 2006;27(4):434–9.
Dagres N, Piorkowski C, Kottkamp H, Kremastinos DT, Hindricks G. Contemporary catheter ablation of arrhythmias in geriatric patients: patient characteristics, distribution of arrhythmias, and outcome. Europace. 2007;9(7):477–80.
Blomström–Lundqvist C, Scheinman MM, Aliot EM, Alpert JS, Calkins H, Camm AJ, et al. ACC/AHA/ESC guidelines for the management of patients with supraventricular arrhythmias––executive summary: a report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines and the European Society of Cardiology Committee for Practice Guidelines (Writing Committee to Develop Guidelines for the Management of Patients With Supraventricular Arrhythmias). Circulation. 2003;108(15):871–909.
Efremidis M, Sideris A, Letsas KP, Alexanian IP, Pappas LK, Mihas CC, et al. Potential–guided versus anatomic–guided approach for slow pathway ablation of the common type atrioventricular nodal reentry tachycardia: a randomized study. Acta Cardiol. 2009;64(4):477–83.
Recibido: 20 de mayo de 2012
Aceptado: 30 de julio de 2012