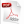CorSalud 2013 Ene-Mar;5(1):57-71
ARTÍCULO ORIGINAL
VALOR PREDICTIVO DE ALGUNOS MODELOS DE ESTRATIFICACIÓN DE RIESGO EN PACIENTES CON INFARTO AGUDO DE MIOCARDIO CON ELEVACIÓN DEL ST
Dra. Queyla M. Cordero Sandovala, Dr. José I. Ramírez Gómezb, MSc. Dr. Francisco L. Moreno-Martínezc, Dr. Osvaldo González Alfonsoc
______________
Servicio de Cardiología. Hospital Privado Salud Integral. Managua, Nicaragua.
Servicio de Cardiología. Hospital Universitario "Arnaldo Milián Castro". Villa Clara, Cuba.
Unidad de Hemodinámica y Cardiología Intervencionista. Cardiocentro "Ernesto Che Guevara". Villa Clara, Cuba.
Correspondencia: FL. Moreno-Martínez. Cardiocentro "Ernesto Che Guevara". Gaveta Postal 350. CP 50100, Santa Clara. Villa Clara, Cuba.
Correo electrónico: flmorenom@yahoo.com
Resumen
Introducción y objetivos: Establecer el pronóstico adecuado en pacientes que han sufrido un infarto de miocardio ha sido una expectativa de los médicos desde tiempos remotos. El objetivo de este estudio fue determinar el valor predictivo de tres modelos de estratificación de riesgo en pacientes con infarto agudo de miocardio con elevación del ST. Método: Se realizó un estudio descriptivo longitudinal en 150 pacientes con esta enfermedad, ingresados en el Servicio de Cardiología del Hospital Provincial Universitario "Arnaldo Milián Castro" de Villa Clara, Cuba, en el período comprendido de enero de 2010 a diciembre de 2011. Resultados: Los pacientes presentaron una edad media de 66,47 años. Predominaron el sexo masculino (62 %) y el infarto de cara inferior (57,3 %). Todos los pacientes complicados o fallecidos fueron clasificados como alto riesgo, según la escala GRACE; y el índice "C" para complicaciones graves y muerte intrahospitalaria tuvo muy buena capacidad predictiva. En el Índice pronóstico, el 57,2 % de los pacientes complicados y el 46,4 % de los fallecidos fueron de alto riesgo, con un índice "C" de 0,67 y 0,65, respectivamente, también existió una pobre capacidad predictiva para ambos eventos. La escala ICR obtuvo un índice "C" de 0,45 para complicaciones graves y 0,41 para mortalidad intrahospitalaria, ambos con muy mala capacidad predictiva. Conclusiones: La escala GRACE presentó muy buena capacidad para predecir complicaciones graves y muerte intrahospitalaria; sin embargo, la escala Índice pronóstico mostró pobre capacidad predictiva para ambos suceso al no clasificar adecuadamente a los pacientes con valores extremos. La escala ICR presentó un índice "C" con mala capacidad predictiva para ambos sucesos.
Palabras clave: Infarto del Miocardio, Medición de Riesgo, Mortalidad Hospitalaria, Complicaciones Cardiovasculares
Abstract
Introduction and Objectives: Establishing appropriate prognosis in patients who have suffered a myocardial infarction has been an expectation of physicians since ancient times. The aim of this study was to determine the predictive value of three risk stratification models in patients with acute myocardial infarction with ST elevation. Method: A longitudinal study was conducted in 150 patients with this disease, admitted to the cardiology department of Arnaldo Milian Castro Provincial University Hospital in Villa Clara, Cuba, from January 2010 to December 2011. Results: Patients had a mean age of 66.47 years. Males (62%) and inferior infarction (57.3%) were predominant. All complicated or dead patients were classified as high risk, according to the GRACE registry, and the "C" index for serious complications and in-hospital death had very good predictive ability. In the prognostic index, 57.2% of patients with complications and 46.4% of deaths were high risk, with a "C" index of 0.67 and 0.65, respectively; there was also a poor predictive ability for both events. The ICR scale obtained a "C" index of 0.45 for severe complications and 0.41 for in-hospital mortality, both with very poor predictive ability. Conclusions: The GRACE registry presented very good ability to predict severe complications and in-hospital death, however, the predictive index scale showed poor prognostic ability for both events by failing to properly classify patients with extreme values. The ICR scale presented a "C" index with poor predictive ability for both events.
Key words: Myocardial Infarction, Risk Assessment, Hospital Mortality, Cardiovascular complications
Introducción
Desde la antigüedad, uno de los objetivos de los médicos ha sido conocer el pronóstico de sus pacientes1. Como reza el aforismo hipocrático, informar adecuadamente del pronóstico al paciente o a su familia puede evitar ser censurado por estos. No obstante, la evaluación del riesgo en los pacientes con un síndrome coronario agudo (SCA) tiene en la actualidad objetivos más amplios que podemos agrupar en 4 apartados1: a) informar y aconsejar al paciente y a su familia; b) identificar a los pacientes con un riesgo elevado de muerte o infarto, susceptibles de mejorar su pronóstico con un tratamiento adecuado; c) identificar a los pacientes con un riesgo muy bajo que no requieren estudios cruentos, lo que evita los costes y los riesgos innecesarios de estas técnicas; y c) planificar la rehabilitación cardíaca y la prevención secundaria tras el episodio agudo2.
Por desgracia, los métodos de evaluación del riesgo en pacientes con SCA distan mucho de la perfección1-4. El pronóstico de los pacientes con un infarto agudo de miocardio (IAM) es muy variable debido a la existencia de una combinación de factores clínicos individuales que están relacionados con un menor o mayor riesgo de presentación de complicaciones cardíacas graves a corto plazo. En la actualidad, algunos avances terapéuticos importantes influyen fundamentalmente en la mortalidad temprana, por lo cual deben ser seleccionados correctamente y aplicados a los subgrupos de mayor riesgo para generar un impacto positivo en los sistemas de salud3.
La auténtica historia natural del IAM con elevación del segmento ST (IAMCEST) es difícil de establecer por una serie de razones: la frecuente incidencia del infarto silente, la frecuencia de la muerte súbita prehospitalaria, y los distintos métodos y definiciones utilizados para el diagnóstico de esta enfermedad. En estudios poblacionales se ha observado, de forma constante, que la tasa total de mortalidad en pacientes con un diagnóstico presumible de IAM o SCA durante el primer mes, es de un 50 %, y alrededor de la mitad de estas muertes ocurren durante las primeras 2 horas5. Esta elevada mortalidad inicial no ha cambiado mucho en los últimos años, a diferencia de lo que ha sucedido con la mortalidad hospitalaria6; donde al contrario de la prehospitalaria, se ha observado un acusado descenso.
Antes de la introducción de las Unidades de Cuidados Coronarios en la década de los sesenta, la mortalidad intrahospitalaria alcanzaba una media de un 25–30 %. En la revisión sistemática de los estudios sobre mortalidad realizados en la era previa a la reperfusión, de mediados de la década de los ochenta, se observó una mortalidad intrahospitalaria de 16 %. Con el uso generalizado de las intervenciones coronarias percutáneas (ICP), los agentes fibrinolíticos, el tratamiento antitrombótico y la prevención secundaria, la mortalidad total al mes se ha reducido a un 4–6 %, al menos en los pacientes participantes en estudios aleatorizados a gran escala y con indicación de fibrinólisis o ICP7,8. No obstante, las tasas reales de mortalidad son mucho más elevadas, lo que indica que los pacientes incluidos en estudios aleatorizados presentan un riesgo menor que los que se encuentran en el "mundo real"9.
Un diagnóstico rápido y la estratificación temprana del riesgo en pacientes que se presentan con dolor torácico agudo son importantes para identificar a los pacientes en quienes una intervención temprana puede mejorar su pronóstico10.
Hay que señalar que la posibilidad de estratificación del riesgo de los pacientes, al usar otros marcadores de riesgo, distintos de los convencionales, no ha sido probada en estudios clínicos importantes11-13.
Algunos de los modelos propuestos intentan predecir el riesgo de muerte a los 30 días por intermedio del análisis de múltiples variables al ingreso, y otras relacionadas con el tratamiento en cohortes de pacientes incluidos en grandes estudios clínicos aleatorizados y controlados que probaron el uso de agentes fibrinolítico4,14-16. Estos modelos nos brindan información útil para una población con similares condiciones clínicas, pero probablemente no siempre igual a la encontrada en la práctica médica diaria. La conformación de un modelo estadístico de ingreso hospitalario, simple y universalmente aplicable, podría clasificar el riesgo, lo que permite un adecuado uso de las estrategias terapéuticas actuales3.
La presencia de enfermedades crónicas no transmisibles en la población cubana va en aumento a medida que se prioriza la atención primaria de salud y el índice de enfermedades transmisibles disminuye, lo que favorece la elevada presencia de enfermedades cardiovasculares. En el año 2009, 22.659 personas murieron por enfermedad cardiovascular y la tasa de muerte por cada 100.000 habitantes fue de 197,82,17.
Mundialmente se señala la capacidad predictiva de los modelos de estratificación de riesgo, especialmente en los SCA, en poblaciones no seleccionadas; pero en Cuba este tipo de estudios son mucho menores2,16,17 y en el Servicio de Cardiología del Hospital "Arnaldo Milián Castro" de Santa Clara solo se ha realizado una investigación previa2, la cual decidimos continuar debido a que no existe aún la aplicación de escalas para predecir el desarrollo de complicaciones y muerte en la población que se atiende.
Los beneficios de esta investigación abarcan los ámbitos científicos y asistenciales al aportar nuevos datos acerca del tema, que permiten optimizar el tratamiento de los pacientes con SCA con elevación del ST, y ayudan a definir estrategias terapéuticas de acuerdo al riesgo, lo que favorece la reducción de complicaciones y la pérdida de recursos económicos para el país2,18.
Por estas razones nos propusimos determinar el valor predictivo de complicaciones graves y muerte intrahospitalarias en tres modelos de estratificación de riesgo en los pacientes con IAMCEST ingresados en el Servicio de Cardiología del mencionado hospital.
Método
Se realizó un estudio descriptivo, longitudinal, prospectivo en 150 pacientes con IAMCEST, durante el período comprendido entre enero de 2010 a diciembre de 2011, ingresados en el Servicio de Cardiología del Hospital Provincial Universitario Clínico Quirúrgico "Arnaldo Milián Castro" de la provincia de Villa Clara, Cuba.
Selección de los pacientes
La población objeto de estudio estuvo constituida por 216 pacientes con IAM atendidos en el Servicio de Cardiología del Hospital, sede durante el período de estudio. La muestra se conformó por 150 pacientes con lAMCEST que cumplieron los criterios de inclusión.
Unidad de análisis: Puntaje de estratificación de riesgo de las escalas del Registro Global de Síndromes Coronarios Agudos (GRACE, por sus siglas en inglés)9,19, InTIME (Intravenous nPA for Treatment of Infarcting Myocardium Early)20,21 e ICR (Instituto Cardiovascular de Rosario)2,3.
Tipo de muestra: No probabilística.
Tipo de muestreo: No probabilístico por conveniencia.
Criterios de inclusión para la muestra:
Diagnóstico de IMACEST.
Pertenecer a la provincia de Villa Clara.
Que el ingreso se haya efectuado en las primeras 24 horas de aparición de los síntomas.
Posibilidad de seguimiento intrahospitalario hasta su egreso.
Los criterios de exclusión se limitan a aquellos pacientes que no cumplieron los criterios de inclusión.
Variables
Se consideró complicación grave (mal traducida en los textos como complicación mayor) a aquella que aparece como complicación directa del IAM, que pone en peligro inmediato la vida del paciente: fallo de bomba con clase de Killip"Kimbal III y IV, arritmia ventricular mantenida, reinfarto, paro cardiorrespiratorio recuperado, complicación mecánica, o necesidad de ICP o tratamiento quirúrgico urgentes.
Se consideró muerte intrahospitalaria a aquella considerada biológica, de carácter irreversible.
Escala de riesgo GRACE22-24
Predice probabilidad de muerte intrahospitalaria y a los 6 meses después del alta hospitalaria. Utiliza las variables: edad, frecuencia cardíaca, presión arterial sistólica, creatinina sérica, clase de Killip, presencia de paro cardiorrespiratorio en el momento del IAM, descenso del ST y elevación de las enzimas cardíacas.
Según el puntaje obtenido por la escala (0–258), los pacientes se estratificaron en tres categorías de riesgo: bajo (≤ 108), intermedio (109–140) y alto (> 140).
Escala de riesgo Índice pronóstico14,20,21,25
El Índice pronóstico es un modelo basado en la fórmula de Morrow14,20 para el subestudio InTIME II, con el objetivo de predecir la posibilidad de muerte a los 30 días, que fue utilizado en una unidad de cuidados intensivos de México21 para valorar, además, la mortalidad en las primeras 24 horas, durante la estancia hospitalaria, en pacientes con IAMCEST. Fue diseñado para calificar el riesgo inicial mediante variables significativas y, a la vez, simples. Su fórmula es: FC (edad/10)2/TAS, donde FC es frecuencia cardíaca y TAS, tensión arterial sistólica.
Las categorías de riesgo son: bajo (< 12,5 puntos), intermedio 1 (12,5–17,5), intermedio 2 (> 17,5–22,5), intermedio 3 (> 22,6–30) y alto (> 30).
Escala de riesgo ICR2,3
La escala ICR fue desarrollada con el propósito de predecir, con variables simples, el riesgo de shock cardiogénico o muerte en la etapa hospitalaria en el IAM. Utiliza cuatro variables: edad, tensión arterial sistólica, frecuencia cardíaca y localización anterior del infarto, y predice la probabilidad de shock cardiogénico y muerte al ingreso hospitalario2,3. Sus categorías de riesgo son: 0 (0–11 puntos) 1 (12–20) y 2 (> 20).

Análisis de la información
Para la realización de la investigación se tomó como fuente primaria de la información el interrogatorio y examen físico de los pacientes estudiados, y como fuente secundaria, la historia clínica hospitalaria.
Las variables obtenidas se almacenaron y analizaron usando el paquete estadístico SPSS para Windows®, 15.0 (SPSS, Chicago, IL, USA).
Para la evaluación de cada una de las escalas se calculó su capacidad de discriminación y calibración. La discriminación se analizó mediante la construcción de la curva COR, que es una función de la sensibilidad y especificidad, y el cálculo del índice «c» o área bajo la curva. La calibración reflejó la capacidad de predecir la aparición de la complicación en estudio en un amplio intervalo de puntuaciones, es decir, la relación entre el riesgo estimado y el real. Para evaluar la calibración se utilizó el método de Hosmer–Lemeshow que califica el valor predictivo del índice, según el área COR en las siguientes categorías1,17:

Para variables cuantitativas determinadas utilizamos como medida de tendencia central la media, y como medida de dispersión, la desviación estándar.
La información obtenida se presenta a través de tablas estadísticas y gráficos con las curvas COR.
Parámetros éticos
Se respetaron los principios éticos y se contó con el consentimiento de la Institución para la realización de esta investigación.
Resultados
El total de pacientes ingresados por SCA en el Servicio de Cardiología del Hospital Universitario "Arnaldo Milián Castro" de Villa Clara durante los años 2010 y 2011 fue de 236 y 294, respectivamente; de manera correspondiente, 93 y 123 pacientes tuvieron un diagnóstico de IAMCEST al egreso. Estos hallazgos hablaban a favor de la necesidad de una investigación científica que abordara la capacidad predictiva de los modelos de estratificación de riesgo de los SCA.
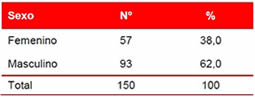
Los pacientes estudiados presentaron una edad media de 66,47 ± 10,95 años, con un mínimo de 38 y un máximo de 94. Predominó el sexo masculino que representó el 62 % de la muestra (Tabla 1).
Tabla 1. Distribución de pacientes, según sexo. Hospital Universitario "Arnaldo Milián Castro". Enero 2010 – Diciembre 2011.
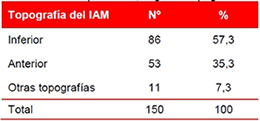
La topografía del infarto en los pacientes estudiados se muestra en la tabla 2. La extensión y localización del miocardio infartado tiene importantes implicaciones pronósticas, en este sentido predominaron los IAM de localización inferior (57,3 %); los anteriores representaron el 35,3 % y el resto (7,3 %), fue de otras topografías.
Tabla 2. Distribución de pacientes, según la topografía del infarto.
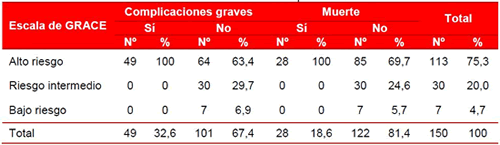
La distribución de los pacientes según la escala GRACE y el desarrollo de complicaciones graves y muerte intrahospitalaria se muestra en la tabla 3. Los 49 pacientes de alto riesgo presentaron complicaciones graves y dentro de los que no las presentaron, el 63,4 % tenía alto riego. Todos los pacientes fallecidos 28 (100 % del total de fallecidos y 18,6 % del total de pacientes) fueron previamente clasificados en el grupo de alto riesgo y de los pacientes con riesgos intermedio y bajo, ninguno presentó complicaciones graves o muerte intrahospitalaria.
Tabla 3. Distribución de pacientes, según la escala GRACE y la aparición de complicaciones graves y muerte intrahospitalaria.
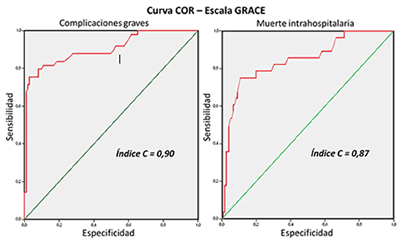
En el gráfico 1 se observa la curva COR determinada para la escala GRACE, según el valor predictivo para complicaciones graves y muerte intrahospitalaria en los pacientes estudiados. Es importante señalar que el índice "C" para las complicaciones (0,90) y la muerte (0,87) tiene valores elevados que evidencian muy buena capacidad predictiva.
Gráfico 1. Validación de la escala GRACE para predecir el desarrollo de complicaciones graves y muerte intrahospitalarias.
De los 49 pacientes que presentaron complicaciones graves, 28 (57,2 %) fueron clasificados como alto riesgo, según la escala Índice pronóstico (Tabla 4); además, fueron incluidos en riesgo intermedio 3, 13 pacientes (26,6 %); intermedio 2, 7 (14,2 %) y en riesgo intermedio 1, solo 1 paciente (2,0 %); sin embargo, todos ellos presentaron complicaciones graves. El Índice pronóstico tiene como propósito principal ajustar el tratamiento del SCA al riesgo individual del paciente; sin embargo, los resultados respecto a la capacidad predictiva de esta escala no fueron los esperados al momento de elaborarse la curva (Gráfico 2).
Tabla 4. Distribución de pacientes, según el Índice pronóstico y la aparición de complicaciones graves y muerte intrahospitalaria.
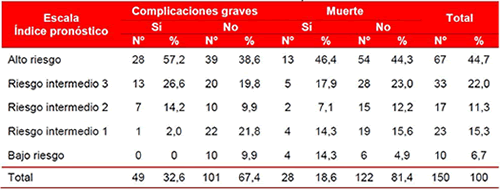
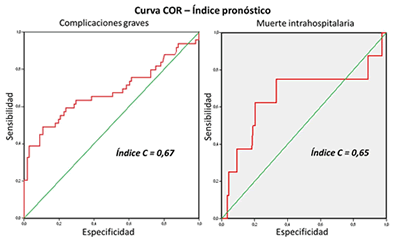
Gráfico 2. Validación de la escala Índice pronóstico para predecir complicaciones graves y muerte intrahospitalarias.
En esta tabla también se puede observar que de los 28 pacientes fallecidos (18,6 %), 13 (46,4 %) fueron clasificados como alto riesgo de muerte intrahospitalaria, según el Índice pronóstico; 5 (17,9 %) fueron incluidos en el grupo de riesgo intermedio 3; 2 (7,1 %) tuvieron un riesgo intermedio 2 y 4 (14,3), un riesgo intermedio 1. Los pacientes con escalas de alto riesgo y riesgo intermedio 3 mostraron un riesgo considerablemente mayor de mortalidad, que al sumar sus porcentajes representan el 66,7 % del total de muertes.
El gráfico 2 muestra las curvas COR del Índice pronóstico con relación a la predicción de complicaciones graves y muerte intrahospitalaria. La validación de este índice mostró una pobre capacidad predictiva, con índices "C" de 0,67 y 0,65, respectivamente.
La tabla 5 presenta la distribución de los pacientes según la escala ICR para el desarrollo de complicaciones graves y muerte intrahospitalaria. Como puede apreciarse, de los 49 pacientes con este tipo de complicaciones (32,6 %), el 55,1 % pertenece a la escala 0, 28,6 % a la escala 1 y el 16,3 % restante, a la escala 2. Observamos como en su mayoría los pacientes que presentaron complicaciones graves fueron incluidos en las escalas 0 y 1 para este modelo de estratificación de riesgo, no correspondiendo de manera real con el riesgo individual que tenía cada paciente, por lo cual no se observa un buen resultado a la hora de realizar su validación. La mayoría de los pacientes eran mayores de 65 años sin embargo, para incluirlos en una escala de 2 debían de encontrarse en su mayoría en etapas iniciales de shock, en correspondencia con los criterios validados para dicha escala.
Tabla 5. Distribución de pacientes, según escala ICR y la aparición de complicaciones graves y muerte intrahospitalaria.
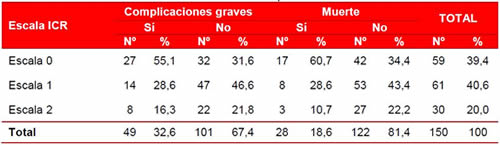
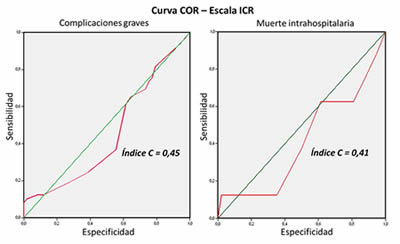
Al analizar la muerte intrahospitalaria, la escala 0 fue la más representativa con 17 pacientes (60,7 %), y en la escala 1 se encontraron 8 (28,6 %), que responden a un número significativo del total de fallecidos. Estos datos nos indican un mal valor predictivo dado la inclusión de la mayoría de los casos en los grupos de menor riesgo, lo cual coincidió con los resultados obtenidos en las curvas COR de dicha escala (Gráficos 3), donde se observa que la validación muestra una mala capacidad predictiva para las complicaciones graves, con un área bajo la curva de 0,45; y 0,41 relacionada con la mortalidad intrahospitalaria.
Gráfico 3. Validación de la escala ICR para predecir complicaciones graves y muerte intrahospitalarias.
Discusión
Existen indicaciones precisas para la reperfusión farmacológica o mecánica en el IAM26-28. El beneficio del tratamiento fibrinolítico está bien establecido29,30; se previenen, aproximadamente, 30 muertes precoces cada 1.000 pacientes tratados antes de las 6 horas de iniciados los síntomas, y 20 muertes por cada 1.000 pacientes tratados entre las 7 y las 12 horas. En general, el beneficio absoluto más elevado se observa en los pacientes con mayor riesgo30-32.
Existe necesidad del uso de escalas de riesgo basadas en parámetros rápidamente identificables en la fase aguda del infarto, con el objetivo de tratar rápidamente al paciente con mayor riesgo de complicaciones graves e incluso de muerte20,28,33. Debido a que el riesgo de complicaciones disminuye con el tiempo, está indicada su valoración temprana.
En la actualidad existen múltiples estudios con el objetivo de facilitar el uso de una escala de estratificación de riesgo que nos ayude a agrupar a los pacientes en un nivel determinado, según su riesgo para establecer así la opción terapéutica más oportuna. En esta investigación evaluamos tres modelos de riesgo: GRACE, Índice pronóstico e ICP.
Otros estudios de estratificación de riesgo3,14 han encontrado resultados similares a los nuestros respecto a la edad y al sexo; además, García Almagro et al.34, encontraron edades de 54 ± 19 años en pacientes con SCA, con mayor prevalencia en el sexo masculino.
Los resultados de Rizo et al.2 también son muy similares, pero decidimos no comparar estos a los nuestros porque, como se dijo anteriormente, esta investigación es continuación de la realizada por los mencionados autores2 dos años antes, en el mismo hospital, con pacientes de igual procedencia sociodemográfica.
La Asociación Estadounidense del Corazón (AHA, por sus siglas en inglés) considera la edad como un predictor de muerte importante en pacientes con IAM, al existir un aumento proporcional entre esta y las tasas de mortalidad informadas. El riesgo de morir se incrementa 1,49 veces por cada 10 años de incremento en la edad34. Lenderink et al.35 valoraron la validez de los indicadores de mortalidad en pacientes ≥ 75 años comparándolo con las escalas TIMI e InTIME, y encontraron que la clase Killip–Kimball III y IV fue el factor de riesgo más importante de mortalidad, y el tiempo de acceso demorado a un servicio de urgencia, la hiperglicemia y la edad avanzada como contribuyentes a un riesgo incrementado, con un índice "C" muy bueno, de 0,86.
Existe una relación entre el número de derivaciones electrocardiográficas con elevación del segmento ST y la mortalidad. Los pacientes con 8 o 9 derivaciones afectadas tienen una mortalidad de 3 a 4 veces superior a aquellos en los que la elevación del ST afecta solo 3 o 4 derivaciones36.
En nuestro estudio la localización más frecuente fue en la cara inferior. Califf et al.37 informaron resultados muy similares, al señalar la cara inferior (58,65 %), como la topografía más frecuente, seguida de la anterior (37,3 %).
La frecuente asociación del IAM anterior con la aparición de complicaciones graves a corto y largo plazos es bien conocida. Los cambios relacionados con el tamaño, forma y grosor ventricular izquierdo, como consecuencia del infarto, afectan no solo el segmento infartado sino a los circundantes (remodelado ventricular), fenómeno influenciado por la carga ventricular, la permeabilidad de la arteria responsable del infarto y su tamaño38. Estos factores intervienen en la función sisto–diastólica del corazón, la cual influye de manera directa en el pronóstico de nuestros pacientes, razón por lo cual en la actualidad la función ventricular izquierda se utiliza en muchos estudios, no solo como importante factor de riesgo para la aparición de complicaciones graves y muerte intrahospitalaria, sino también para la evaluación y estratificación del riesgo a corto y largo plazos39.
Raposeiras–Roubín et al.40 señalan que los IAM de localización anterior tienen dos veces más probabilidades de morir que los que tienen un infarto inferior, debido a su asociación frecuente con el shock cardiogénico. La probabilidad de presentar síntomas clínicos que evolucionen al shock cardiogénico y la muerte se relaciona con parámetros específicos de la función ventricular izquierda39-43. El conocimiento de estos aspectos apoya el uso de diferentes escalas de estratificación de riesgo, dada la relación existente entre la arteria responsable del infarto, su tamaño y la posibilidad de complicaciones eléctricas graves que comprometen la vida del enfermo desde el inicio del proceso isquémico, o la presencia de deterioro hemodinámico y complicaciones mecánicas con la necesidad de intervención quirúrgica oportuna44-46.
Desde hace dos décadas, distintos modelos que provienen de las matemáticas aplicadas, la estadística, y otras ciencias, han contribuido a que las predicciones que habitualmente realizamos sobre la futura evolución de los pacientes, se vean ayudadas por métodos cuantitativos que permiten, aunque con ciertas limitaciones, dar valores numéricos a nuestras predicciones, y así poder tomar, en muchos casos, decisiones más racionales y efectivas2,47. Con este propósito surgen las escalas de riesgo, que podrían definirse como un algoritmo o regla de predicción clínica, y ayudan al médico a interpretar la información obtenida2,3,48.
El hecho de encontrar que el 32,6 % de los pacientes desarrollaron complicaciones graves y que, inicialmente todos ellos fueron incluidos en el grupo de alto riesgo según la escala GRACE, permitió efectuar la intervención terapéutica más oportuna, lo que favorece la evolución y el pronóstico a corto y largo plazos. Consideramos que los resultados alcanzados pueden estar en relación con el amplio rango de valores ofrecidos por esta escala, lo que facilita la posibilidad de poder incluir más características individuales no solo en correspondencia con el SCA, sino también con las comorbilidades asociadas que pudieran afectar paralelamente al paciente.
El estudio GRACE es un registro multinacional, que incluye pacientes con SCA, cuyo objetivo principal es mejorar la calidad y expectativa de vida, así como describir estrategias de diagnóstico y tratamiento adecuados en pacientes con este tipo de enfermedad22-24.
Granger et al.49, a través de un análisis de regresión logística múltiple, realizaron un modelo para evaluar la probabilidad de muerte intrahospitalaria en 11.380 pacientes, el cual fue validado en una cohorte prospectiva de 3.972 pacientes; de igual manera fueron evaluados 12.142 pacientes del estudio GUSTO IIb. En ambos estudios los factores de riesgo y el nivel pronóstico encontrados, relacionados con la escala GRACE, fueron similares a nuestros resultados; al igual que los encontrados por Araujo–Gonçalves et al.46; sin embargo, otros estudios2,50 sugieren que la escala GRACE pierde parte de su capacidad de discriminación cuando se aplica en una población diferente, menos seleccionada.
En nuestra investigación las curvas COR de esta escala mostraron buena sensibilidad y especificidad para predecir complicaciones graves y muerte intrahospitalaria. Fox et al.19 señalan que la confiabilidad predictiva del modelo GRACE es buena, con una "C" estadística de 0,82 para muerte intrahospitalaria, y tiene en cuenta nueve factores que se asocian con un valor predictivo independiente de los criterios principales de análisis entre el momento de internación y a los 6 meses, estos son: edad, insuficiencia cardíaca congestiva, enfermedad vascular periférica, presión arterial sistólica, clase de Killip, concentración sérica inicial de creatinina, marcadores cardíacos positivos al inicio, paro cardíaco en el momento de la internación y número de derivaciones con desviación del ST.
Es importante señalar que, según este mismo autor19, algunos grupos consideran que el modelo de mortalidad que surgió del estudio GRACE49 es superior al TIMI o al modelo propuesto por Boersma et al.51, por su buen poder de predicción de riesgo acumulado en pacientes con diferentes SCA, que se asocia con una validez prospectiva y externa. Por su parte, el modelo simplificado brinda la mayor parte de la información y es aplicable en pacientes individuales.
A pesar de la buena capacidad predictiva y de la fácil aplicación de la escala GRACE, su utilización está muy limitada en la práctica clínica. Datos del propio registro GRACE2,19,49 demuestran que la utilización de ICP en pacientes con SCA es independiente al riesgo estimado, pues en pacientes con SCA con elevación del segmento ST y riesgo bajo se practicó ICP en el 60 % de los casos, en comparación con el 41 % de los pacientes con alto riesgo. Datos similares se obtuvieron en el registro DESCARTES2,3,52, en los que el pronóstico de pacientes con IAMCEST, estimado mediante la puntuación TIMI, no influía en la decisión de realizar ICP. No obstante, estas observaciones nada tienen en contra de la escala mencionada, simplemente es una muestra de la poca adherencia a ella para definir la conducta a seguir ante el enfermo.
Por otra parte, el estudio de Eagle et al.53 puede servir de alerta para no olvidar que en pacientes con SCA el índice de Killip y Kimbal posee un importante valor predictivo independiente. Por este motivo parece razonable sugerir que no debe ser olvidada la incorporación de sencillas mediciones de la función ventricular dentro de las escalas desarrolladas para la evaluación del riesgo. En nuestra investigación el 65,5 % de los pacientes complicados presentaron una clase funcional III o IV.
Datos publicados por Rathore et al.25 señalan que el 48,69 % de los casos complicados fueron previamente clasificados como alto riesgo, según la escala GRACE, lo que coincide con nuestros resultados. Igual sucede al predecir la mortalidad, donde se plantea que la letalidad a los 30 días fue de 21,7 %, muy similar a la encontrada en nuestra investigación.
La pobre capacidad predictiva de la escala del Índice pronóstico para predecir el desarrollo de complicaciones graves (0,60) y muerte intrahospitalaria (0,69), fue similar a la encontrada por otros autores14,25. Aunque este índice parece tener un buen desempeño en poblaciones pequeñas, tiene limitaciones cuando es aplicado para una cohorte basada en comunidades de pacientes de edad avanzada2, lo cual sugiere que esta escala de riesgo funciona pobremente cuando es utilizada en una cohorte nacionalmente representativa25.
Llama la atención que los pacientes que se ubicaron en escalas intermedias, según el Índice pronóstico, no presentaron una relación directa entre estas y el riesgo de muerte, por lo que pudiéramos plantear que este índice, basado en la fórmula de Morrow14,20, define y estratifica adecuadamente la probabilidad de muerte para los pacientes con valores extremos, pero no para los intermedios.
La escala ICP fue desarrollada con el propósito de predecir, con variables simples (edad, tensión arterial sistólica, frecuencia cardíaca y localización anterior del IAM), el riesgo de presentar shock cardiogénico o muerte en la etapa hospitalaria del IAM3. Zapata et al.3 plantean que los valores 0, 1 y 2 mostraron una tasa de shock o muerte intrahospitalaria de 2,7 %, 15,5 % y 59,4 %, con una buena calibración del modelo y un área bajo la curva COR de 0,80, que se corresponde con una buena discriminación para sensibilidad y especificidad en el grupo de pacientes incluidos en ese estudio, lo cual no coincide con nuestros resultados. Contrario a lo planteado por este autor3, la escala ICR no fue efectiva para predecir complicaciones graves y riesgo de muerte intrahospitalaria en poblaciones no específicas, pues encontramos un índice "C" con muy mala capacidad predictiva, lo que evidencia una mala predicción del suceso, debido a sus escasas sensibilidad y especificidad.
Es preciso señalar que aunque se han desarrollado excelentes ensayos clínicos, los resultados son susceptibles de distintas interpretaciones y que la finalidad de estos es dar lugar a una intervención temprana, y proporcionar opciones de tratamiento a los pacientes que están determinados de manera directa por el riesgo individual de cada uno de ellos y, en parte, por los recursos disponibles en el centro donde se les preste atención.
Somos conscientes de que las pruebas diagnósticas y las opciones de tratamiento pueden no estar disponibles en todas las instituciones o países, incluso en los países más ricos; las cuestiones relativas al coste–efectividad tienen cada vez más importancia a la hora de decidir sobre estrategias terapéuticas. Como hasta ahora, las guías de práctica clínica no son prescriptivas, entre un paciente y otro existen muchas diferencias, por lo que la atención individualizada es de suma importancia; y el juicio clínico, la experiencia y el sentido común ocupan lugares muy importantes.
El valor pronóstico de la función ventricular en pacientes con enfermedades cardiovasculares agudas o crónicas está ampliamente comprobado, así como la utilidad de su evaluación por medios clínicos o por imágenes (ecocardiografía) para estratificar el riesgo y facilitar la toma de decisiones. Algunas de las escalas de predicción propuestas no incluyen mediciones de la función ventricular, ya sea por medios clínicos o por imágenes. Esto seguramente ha limitado su utilidad y puede, en parte, justificar los bajos valores de índice "C" observados con algunos modelos propuestos49.
Desde hace varios años la determinación de proteínas intracelulares y marcadores inflamatorios, como las troponinas, la proteína C reactiva y el péptido natriurético cerebral (BNP o NT-pro BNP, por sus siglas en inglés) ha cobrado gran auge en diversos ensayos clínicos aleatorizados, razón por la cual ha surgido gran entusiasmo en la comunidad médica, debido a que son útiles para estratificar el pronóstico, al identificar a los pacientes con mayor riesgo de complicaciones fatales que no podrían detectarse por los medios habituales24,54. Probablemente su inclusión en los modelos de predicción de riesgo aumenten la capacidad predictiva de estos; no obstante, si bien los resultados conocidos hasta el momento son alentadores, antes de incluir estos marcadores en las escalas de riesgo, hacen falta otros estudios que ajusten el valor predictivo real de cada uno de ellos en las diferentes poblaciones11-13,55,56; así como también analizar las relaciones costo–beneficio, costo–eficacia y costo–efectividad57,58; pues aunque algunas de las modalidades terapéuticas más eficaces (balón de contrapulso intraaórtico, angioplastia, revascularización quirúrgica urgente), sólo pueden llevarse a cabo en centros de atención terciaria de salud, los centros de escasos recursos tendrán la posibilidad de identificar rápidamente a los pacientes de mayor riesgo para poder transferirlos a instituciones de mayor desarrollo.
Aunque solo se comentan algunos de los factores más comunes, no se debe olvidar que el SCA es una enfermedad en la cual, desde el punto de vista fisiopatológico, intervienen múltiples factores que afectan en mayor o menor medida a diversos sistemas del organismo; por eso los modelos de estratificación de riesgo deben nutrirse continuamente, pues los avances en las estrategias terapéuticas en las últimas décadas permiten ofrecer a los pacientes diferentes opciones de tratamientos, en función de la gravedad de la enfermedad y su pronóstico.
Conclusiones
De los tres modelos de estratificación de riesgo en pacientes con IAMCEST, la escala de riesgo GRACE exhibió mayor sensibilidad y especificidad para predecir la aparición de complicaciones graves y muerte intrahospitalaria. El Índice pronóstico definió y estratificó adecuadamente la probabilidad de muerte para pacientes encontrados en valores extremos, no así, para los incluidos en rangos intermedios; y con la escala ICR no se obtuvieron buenos índices predictivos.
Referencias bibliográficas
Sanz G. Estratificación del riesgo en los síndromes coronarios agudos: un problema no resuelto. Rev Esp Cardiol [Internet]. 2007 [citado 2010 Nov 12];60(Supl 3):23–30.
Rizo GO, Ramírez JI, Pérez D, Novo L, Acosta F, Cordero Q, et al. Valor predictivo de muerte y complicaciones intrahospitalarias de los modelos de estratificación de riesgo en pacientes con infarto miocárdico agudo. Rev Fed Arg Cardiol. 2011;40(1):57–64.
Zapata G, Lasave L, Tuero E, Orlandini A, Paolasso E. Desarrollo de un modelo simple para clasificar el riesgo al ingreso hospitalario en el infarto agudo de miocardio (SCORE ICR). Rev Fed Arg Cardiol. 2003;32:506–10.
Ottenvanger JP, Armstrong P, Barnathan ES, Boersma E, Cooper JS, Ohman EM, et al. For the GUSTO IV–ACS Investigators. Longterm results after the glycoprotein IIb/IIIa inhibitor abciximab in unstable angina. Circulation 2003;107(3):437–42.
Keeley EC, Boura JA, Grines CL. Comparison of primary and facilitated percutaneous coronary interventions for ST–elevation myocardial infarction: quantitative review of randomised trials. Lancet. 2006;367(9510):579–88.
Goldberg RJ, Glatfelter K, Burbank–Schmidt E, Lessard D, Gore JM. Trends in community mortality due to coronary heart disease. Am Heart J. 2006;151(2):501–7.
APEX AMI Investigators, Armstrong PW, Granger CB, Adams PX, Hamm C, Holmes D, et al. Pexelizumab for acute ST–elevation myocardial infarction in patients undergoing primary percutaneous coronary intervention: a randomized controlled trial. JAMA. 2007;297(1):43–51.
Assessment of the Safety and Efficacy of a New Treatment Strategy with Percutaneous Coronary Intervention (ASSENT–4 PCI) investigators. Primary versus tenecteplase–facilitated percutaneous coronary intervention in patients with ST–segment elevation acute myocardial infarction (ASSENT–4 PCI): randomised trial. Lancet 2006;367(9510):569–78.
Fox KA, Dabbous OH, Goldberg RJ, Pieper KS, Eagle KA, Van de Werf F, et al. Prediction of risk of death and myocardial infarction in the six months after presentation with acute coronary syndrome: prospective multinational observational study (GRACE). BMJ. 2006;333(7578):1091–4.
Le May MR, So DY, Dionne R, Glover CA, Froeschl MP, Wells GA, et al. A citywide protocol for primary PCI in ST segment elevation myocardial infarction. N Engl J Med. 2008;358(3):231–40.
Henkel DM, Witt BJ, Gersh BJ, Jacobsen SJ, Weston SA, Meverden RA, et al. Ventricular arrhythmias after acute myocardial infarction: a 20–year community study. Am Heart J. 2006;151(4):806–12.
Zipes DP, Camm AJ, Borggrefe M, Buxton AE, Chaitman B, Fromer M, et al. ACC/AHA/ESC 2006 guidelines for management of patients with ventricular arrhythmias and the prevention of sudden cardiac death–executive summary: a report of the American College of Cardiology/American Heart Association Task Force and the European Society of Cardiology Committee for Practice Guidelines (Writing Committee to Develop Guidelines for Management of Patients with Ventricular Arrhythmias and the Prevention of Sudden Cardiac Death) developed in collaboration with the European Heart Rhythm Association and the Heart Rhythm Society. Eur Heart J. 2006;27(17):2099–140.
Vardas PE, Auricchio A, Blanc JJ, Daubert JC, Drexler H, Ector H, et al. Guidelines for cardiac pacing and cardiac resynchronization therapy: The task force for cardiac pacing and cardiac resynchronization therapy of the European Society of Cardiology. Developed in collaboration with the European Heart Rhythm Association. Eur Heart J. 2007;28(18):2256–95.
Morrow DA, Antman EM, Charlesworth A, Cairns R, Murphy SA, De Lemos JA, et al. TIMI risk score for ST–elevation myocardial infarction: a convenient, bedside, clinical score for risk assessment at presentation. An Intravenous nPA for treatment of infarcting myocardium early II trial substudy. Circulation. 2000;102(17):2031–7.
Nallamothu B, Fox KA, Kennelly BM, Van de Werf F, Gore JM, Steg PG, et al. Relationship of treatment delays and mortality in patients undergoing fibrinolysis and primary percutaneous coronary intervention. The Global Registry of Acute Coronary Events. Heart. 2007;93(12):1552–5.
Alonso Mariño AL, Alonso Marino OL, Grau Ávalos R. Infarto agudo de miocardio en pacientes jóvenes ingresados en cuidados intensivos. CorSalud. 2012;4(1):20–9. Disponible en: http://bvs.sld.cu/revistas/cors/pdf/2012/v4n1a12/es/iam.pdf
Almeida Gómez J, Rivero Varona MM, Méndez Peralta T, Sterling Duarte J, Valdés Recarey M. Valor pronóstico de factores obtenidos por métodos no invasivos en el infarto agudo del miocardio. Rev Cubana Med [Internet]. 2007 [citado 20 Jul 2011];46(1):[aprox. 10 p]. Disponible en: http://scielo.sld.cu/scielo.php?pid=S0034–75232007000100005&script=sci_arttext
Zapata G. Predicción temprana del riesgo en el infarto agudo de miocardio: una difícil tarea de todos los días. Rev Fed Arg Cardiol. 2011;40(1):1–2.
Fox KA, Eagle KA, Gore JM, Steg PG, Anderson FA; GRACE and GRACE2 Investigators. The global registry of acute coronary events, 1999 to 2009––GRACE. Heart. 2010;96(14):1095–101
Morrow DA, Antman EM, Giugliano RP, Cairns R, Charlesworth A, Murphy SA, et al. A simple risk index for rapid initial triage of patients with ST–elevation myocardial infarction: an InTIME II substudy. Lancet. 2001;358(9293):1571–5.
Esquivel CG, Chávez L, Albarrán J, Ramírez JR, Flores E, Martínez JA, et al. Índice pronóstico de infarto agudo de miocardio con elevación–ST en la unidad de cuidados intensivos. Med Int Mex. 2008;24(1):22–7.
Tang EW, Wong CK, Herbison P. Global Registry of Acute Coronary Events (GRACE) hospital discharge risk score accurately predicts long–term mortality post–acute coronary syndrome. Am Heart J. 2007;153(1):29–35.
Widera C, Pencina MJ, Meisner A, Kempf T, Bethmann K, Marquardt I, et al. Adjustment of the GRACE score by growth differentiation factor 15 enables a more accurate appreciation of risk in non–ST–elevation acute coronary syndrome. Eur Heart J. 2012;33(9):1095–104.
Khan SQ, Narayan H, Ng KH, Dhillon OS, Kelly D, Quinn P, et al. N–terminal pro–B–type natriuretic peptide complements the GRACE risk score in predicting early and late mortality following acute coronary syndrome. Clin Sci (Lond). 2009;117(1):31–9.
Rathore SS, Weinfurt KP, Gross CP, Krumholz HM. Validity of a simple ST–elevation acute myocardial infarction risk index. Circulation 2003;107(6):811–6.
Bataille Y, Déry JP, Larose E, Déry U, Costerousse O, Rodés–Cabau J, et al. Deadly association of cardiogenic shock and chronic total occlusion in acute ST–elevation myocardial infarction. Am Heart J. 2012;164(4):509–15.
Tayara W, Starling RC, Yamani MH, Wazni O, Jubran F, Smedira N. Improved survival after acute myocardial infarction complicated by cardiogenic shock with circulatory support and transplantation: comparing aggressive intervention with conservative treatment. J Heart Lung Transplant. 2006;25(5):504–9.
Hochman JS, Lamas GA, Buller CE, Dzavik V, Reynolds HR, Abramsky SJ, et al. Coronary intervention for persistent occlusion after myocardial infarction. N Engl J Med. 2006;355(23):2395–407.
White HD. Thrombolytic therapy in the elderly. Lancet. 2000;356(9247):2028–30.
Morrison LJ, Verbeek PR, McDonald AC, Sawadsky BV, Cook DJ. Mortality and prehospital thrombolysis for acute myocardial infarction: a meta–analysis. JAMA. 2000;283(20):2686–92.
Kalla K, Christ G, Karnik R, Malzer R, Norman G, Prachar H, et al. Implementation of guidelines improves the standard of care: the Viennese registry on reperfusion strategies in ST–elevation myocardial infarction (Vienna STEMI registry). Circulation. 2006;11(20)3:2398–405.
Danchin N, Coste P, Ferrières J, Steg PG, Cottin Y, Blanchard D, et al. Comparison of thrombolysis followed by broad use of percutaneous coronary intervention with primary percutaneous coronary intervention for ST–segment–elevation acute myocardial infarction: data from the french registry on acute ST–elevation myocardial infarction (FAST–MI). Circulation. 2008;118:268–76.
Thiele H, Smalling RW, Schuler GC. Percutaneous left ventricular assist devices in acute myocardial infarction complicated by cardiogenic shock. Eur Heart J. 2007;28(3):2057–63.
García Almagro FJ, Gimeno JR, Villegas M, Muñoz L, Sánchez E, Teruel F, et al. Aplicación de una puntuación de riesgo coronario (TIMI Risk Score) en una población no seleccionada de pacientes que consultan por dolor torácico en un servicio de urgencias. Rev Esp Cardiol. 2005;58(7):775–81.
Lenderink T, Hernández AV, Boersma E, Martínez–Sellés M, Juárez M, Sánchez PL, et al. Prediction of 30–day mortality in older patients with a first acute myocardial infarction. Cardiology. 2010;115(1):1–9.
Krucoff MW, Johanson P, Baeza R, Crater SW, Dellborg M, et al. The clinical utility of serial and continuos ST–segment recovery in patients with acute elevation myocardial infarction: Assesing the dynamics of epicardial and myocardial reperfusion. Circulation. 2004;110(25):e533–9.
Califf RM, Pieper KS, Lee KL, Van De Werf F, Simes RJ, Armstrong PW, et al. Prediction of 1–year survival after thrombolysis for acute myocardial infarction in th global utilization of streptokinase and TPA for occluded coronary arteries trial. Circulation. 2000;101(19):2231–8.
Shah RV, Holmes D, Anderson M, Wang TY, Kontos MC, Wiviott SD, et al. Risk of heart failure complication during hospitalization for acute myocardial infarction in a contemporary population: Insights from The National Cardiovascular Data ACTION Registry. Circ Heart Fail. 2012;5(6):693–702.
de Boer SP, Barnes EH, Westerhout CM, Simes RJ, Granger CB, Kastrati A, et al. High–risk patients with ST–elevation myocardial infarction derive greatest absolute benefit from primary percutaneous coronary intervention: Results from the Primary Coronary Angioplasty Trialist versus Thrombolysis (PCAT)–2 Collaboration. Am Heart J. 2011;161(3):500–7.e1.
Raposeiras–Roubín S, Abu–Assi E, Cabanas–Grandío P, Agra–Bermejo RM, Gestal–Romarí S, Pereira–López E, et al. Walking Beyond the GRACE (Global Registry of Acute Coronary Events) Model in the Death Risk Stratification During Hospitalization in Patients With Acute Coronary Syndrome: What Do the AR–G (ACTION [Acute Coronary Treatment and Intervention Outcomes Network] Registry and GWTG [Get With the Guidelines] Database), NCDR (National Cardiovascular Data Registry), and EuroHeart Risk Scores Provide? JACC Cardiol Intv. 2012;5(11):1117–25.
Peacock WF, Soto–Ruiz KM. Risk stratification for suspected acute coronary syndromes and heart failure in the emergency department. Acute Card Care. 2009;11(3):138–45.
Verma A, Pfeffer MA, Skali H, Rouleau J, Maggioni A, McMurray JJ, et al. Incremental value of echocardiographic assessment beyond clinical evaluation for prediction of death and development of heart failure after high–risk myocardial infarction. Am Heart J. 2011;161(6):1156–62.
Erlikh AD. A scale for early assessment of risk of death and myocardial infarction during initial hospitalization of patients with acute coronary syndromes (based on data from the RECORD registry). Kardiologiia. 2010;50(10):11–6.
Wood AM, Greenland P. Evaluating the prognostic value of new cardiovascular biomarkers. Dis Markers. 2009;26(5–6):199–207.
Kozieradzka A, Kaminski KA, Maciorkowska D, Olszewska M, Dobrzycki S, Nowak K, et al. GRACE, TIMI, Zwolle and CADILLAC risk scores––do they predict 5–year outcomes after ST–elevation myocardial infarction treated invasively? Int J Cardiol. 2011;148(1):70–5.
de Araujo–Gonçalves P, Ferreira J, Aguiar C, Seabra–Gómez R. TIMI, PURSUIT, and GRACE risk scores: sustained prognostic value and interaction with revascularization in NSTE–ACS. Eur Heart J. 2005;26(9):865–72.
Carrillo N. Uso de modelos matemáticos para aplicaciones biomédicas [Internet]. 2011 [citado 8 Sept 2012]. Disponible en: http://www.electronicosonline.com/2011/01/04/uso–de–modelos–matematicos–para–aplicaciones–biomedicas/
Núñez E, Steyerbergc EW, Núñez J. Estrategias para la elaboración de modelos estadísticos de regresión. Rev Esp Cardiol. 2011;64(6):501–7
Granger CB, Goldberg RJ, Dabbous O, Pieper KS, Eagle KA, Cannon CP, et al. Predictors of hospital mortality in the global registry of acute coronary events. Arch Intern Med. 2003;163 (19):2345–53.
Yan AT, Jong P, Yan RT, Tan M, Fitchett D, Chow CM, et al. Clinical trial–derived risk model may not generalize to real–world patients with acute coronary sindrome. Am Heart J. 2004;148(6):1020–7.
Boersma E, Pieper KS, Steyerberg EW, Wilcox RG, Chang WC, Lee KL, et al. Predictors of outcome in patients with acute coronary syndromes without persistent ST–segment elevation. Results from an international trial of 9461 patients. The PURSUIT investigators. Circulation 2000;101(22):2557e67.
Bueno H, Bardají A, Fernández–Ortiz A, Marrugat J, Martí H, Heras M. Management of non–ST–segment–elevation acute coronary syndromes in Spain. The DESCARTES (Descripción del Estado de los Síndromes Coronarios Agudos en un Registro Temporal ESpañol) study. Rev Esp Cardiol. 2005;58(3):244–52.
Eagle KA, Lim MJ, Dabbous OH, Pieper KS, Goldberg RJ, Van de Werf F, et al. A validated predicition model for all forms of acute coronary syndrome. JAMA. 2004;291:2727–33.
Khan SQ, Ng K, Dhillon O, Kelly D, Quinn P, Squire IB, et al. Growth differentiation factor–15 as a prognostic marker in patients with acute myocardial infarction. Eur Heart J. 2009;30(9):1057–65.
Anselmino M, Bartnik M, Malmberg K, Rydén L. Management of coronary artery disease in patients with and without diabetes mellitus. Acute management reasonable but secondary prevention unacceptably poor: a report from the Euro Heart Survey on Diabetes and the heart. Eur J Cardiovasc Prev Rehabil. 2007;14:28–36.
Graham I, Atar D, Borch–Johnsen K, Boysen G, Burell G, Cifkova R, et al. European guidelines on cardiovascular disease prevention in clinical practice: executive summary. Fourth Joint Task Force of the European Society of Cardiology and other societies on cardiovascular disease prevention in clinical practice (constituted by representatives of nine societies and by invited experts). Eur Heart J. 2007;14 Suppl 2:E1–40.
Scirica BM, Sabatine MS, Jarolim P, Murphy SA, de Lemos JL, Braunwald E, et al. Assessment of multiple cardiac biomarkers in non–ST–segment elevation acute coronary syndromes: observations from the MERLIN–TIMI 36 trial. Eur Heart J. 2011;32(6):697–705.
Giugliano RP, Pollack CV, Brogan GX, Cohen M, Diercks DB, Grines CL, et al. Acute Coronary Syndromes: From the Emergency Department to the Catheterization Laboratory–Integrating Evidence from Recent ACS/NSTEMI Trials into Clinical Practice: An Evidence–Based Review of Recent Clinical Trial Results and Report on a Roundtable Discussion. J Interv Cardiol. 2011;24(2):119–36.
Recibido: 31 de mayo de 2012
Recibido con modificaciones: 23 de julio de 2012
Aceptado: 25 de septiembre de 2012