CorSalud 2015 Abr-Jun;7(2):135-140
ARTÍCULO DE REVISIÓN
DUCTUS ARTERIOSO: ECOANATOMÍA Y MECANISMOS DE CIERRE
Dr. Carlos García Guevaraa, Dr. Guillermo Schvartzb, Dr. Manuel Melnikc, Dr. William García Lugod, Dra. Jakeline Arencibia Faifea, Dr. Andrés Savío Benavidesa, Dr. Carlos García Morejóna
______________
Cardiocentro Pediátrico "William Soler". La Habana, Cuba.
Hospital de Niños Ricardo Gutiérrez. Buenos Aires, Argentina.
Universidad de la República (Regional Norte) UDELAR. Salto, Uruguay.
Universidad de Ciencias Médicas de La Habana. Facultad Enrique Cabrera. La Habana, Cuba.
Correspondencia: C García Guevara. Cardiocentro Pediátrico William Soler. Ave. 100 y Perla, Alta Habana. Boyeros, CP 10800. La Habana, Cuba. Correo electrónico: carlos.guevara@infomed.sld.cu
Resumen
El ductus arterioso es una estructura anatómica esencial en la vida del feto, que permite ser manipulado farmacológicamente y, de no completarse su cierre funcional y anatómico en la etapa de recién nacido, se considera una cardiopatía congénita. Su importancia fue motivo para efectuar la presente revisión, donde se tratan aspectos relacionados con la embriología, anatomía y función de esta estructura, ilustrados con imágenes ecocardiográficas de fetos estudiados en el Servicio de Cardiología Fetal del Cardiocentro Pediátrico William Soler, en las que se observan las vistas clásicas utilizadas en su estudio, y ejemplos de anomalías diagnosticadas, con el objetivo de ofrecer información resumida acompañada de nuestra experiencia en la evaluación del ductus, así como el diagnóstico de algunas de sus anomalías.
Palabras clave: Ductus arterioso, Ecocardiografía fetal, Diagnóstico prenatal, Cardiopatías congénitas
Ductus Arteriosus: Ecographic anatomy and closure mechanisms
Abstract
Ductus arteriosus is an essential anatomical structure in the life of the fetus, which can be treated pharmacologically; and, if its functional and anatomic closure is not completed in the newborn stage, it is considered a congenital heart defect. Its importance motivated us to conduct this review, which deals with aspects related to the embryology, anatomy and function of this structure. It is illustrated with echocar-diographic images of fetuses, which were studied at the Fetal Cardiology Department of the William Soler Pediatric Cardiology Hospital, showing the classical views used in its study, and examples of diagnosed anomalies, with the aim of providing summa-rized information together with our experience in the assessment of ductus and the diagnosis of some of its anomalies.
Key words: Ductus arteriosus, Fetal echocardiography, Prenatal diagnosis, Congenital heart disease
Introducción
El ductus arterioso (DA) es un estructura vascular que conecta la aorta descendente proximal con el techo de la arteria pulmonar principal, cerca del origen de la arteria pulmonar izquierda1. Fue descrita por primera vez en el feto por Galeno (129-200), quien incluso habló de su cierre posnatal en el siglo II2-3. La primera mención del término ductus arteriosus apareció en un libro de Arantii Iulii Caesaris, De humano foetu libellus, publicado en 1595. Allí él menciona el ductus venoso y el arterial4; más tarde, en 1628, William Harvey describió la orientación del flujo sanguíneo a través de él en la vida fetal5, y Virchow sugirió que el cierre del ductus era secundario a la contracción del músculo liso existente en su pared. Según Marquis6, fue reconocido como enfermedad aislada, con la descripción de Rokitansky, en 1844 y 1852.
La importancia de esta estructura en la vida fetal y los aspectos fundamentales que sobre su embriología, anatomía ecocardiográfica y sus mecanismos de cierre se han publicado, fueron motivo para realizar la presente revisión, que se ilustra con imágenes de estudios realizados en el Servicio de Cardiología Fetal del Cardiocentro Pediátrico William Soler, Centro de Referencia Nacional para el diagnóstico de las cardiopatías congénitas en el feto y la cirugía cardiovascular en el paciente menor de un año, en Cuba.
ANATOMÍA EMBRIONARIA
En la porción cefálica del embrión, a lo largo de la pared ventral y lateral del intestino faríngeo, aparecen los arcos faríngeos con una secuencia céfalo-caudal. Dichos arcos faríngeos son barras de tejido mesenquimal separados por fuera por las hendiduras faríngeas. Del mismo modo, las bolsas faríngeas, que también aparecen en las paredes laterales del intestino del mismo nombre, separan los arcos faríngeos uno del otro. A lo largo de la pared dorsal del embrión, a ambos lados de este intestino, aparecen dos arterias: las aortas dorsales derecha e izquierda, y en frente de la pared ventral del intestino está el saco aórtico, el cual se continúa con el truncus. A medida que cada arco faríngeo aparece, el saco aórtico contribuye con ramas arteriales derechas e izquierdas, y se constituyen seis pares de arterias denominadas arcos aórticos. Estos arcos unen al saco aórtico con las aortas dorsales derecha e izquierda, respectivamente. La aorta ascendente se origina del saco aórtico, la porción transversa del cuarto arco aórtico izquierdo y la descendente de la aorta dorsal izquierda. Cuando el saco aórtico es divido por el septum aórtico-pulmonar en aorta ascendente y tronco de la arteria pulmonar, el sexto arco pierde conexión con la aorta y queda conectado con el tronco pulmonar. En el lado derecho, la porción ventral del sexto arco aórtico finalmente deviene en la porción proximal de la arteria pulmonar derecha, mientras que la porción dorsal desaparece. En el lado izquierdo, la porción ventral es absorbida dentro del tronco pulmonar y el segmento dorsal deviene en el DA. Esto nos hace comprender por qué el ductus une el tronco de la arteria pulmonar en su techo, cerca del origen de las ramas pulmonares, con la porción proximal de la aorta descendente7,8.
Cuando el cayado aórtico es derecho y el ductus izquierdo, este unirá al tronco de la arteria pulmonar con la subclavia izquierda aberrante, lo que hace que pueda pasar por delante o por detrás de la tráquea, en cuyo caso se forma un anillo vascular9 (Figura 1). También puede existir doble DA en casos con obstrucción grave al flujo pulmonar y en algunos casos de doble arco aórtico10,11.
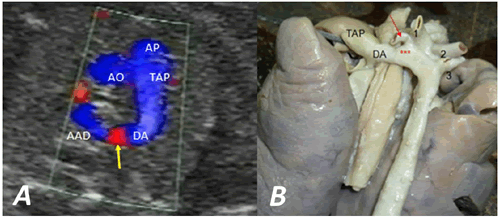
Figura 1. A. Imagen ecocardiográfica y B. Vista posterior de una pieza anatómica donde se aprecian un arco aórtico derecho con ductus izquierdo, este último une la porción proximal de la rama pulmonar izquierda con la porción proximal de la arteria subclavia izquierda aberrante, y pasa por detrás de la tráquea. AAD: arco aórtico derecho, AO: arteria aorta, AP: arteria pulmonar, DA: ductus arterioso, TAP: tronco de la arteria pulmonar, 1: tronco braquiocefálico izquierdo, 2: carótida derecha, 3: subclavia derecha, ***: divertículo de Kommerell. La flecha señala la arteria carótida izquierda aberrante.
ECOCARDIOGRAFÍA
La visualización del DA puede ser valorada al realizar diferentes cortes ecocardiográficos en el feto a través de varias vistas10-15:
Corte transversal del feto: específicamente en la vista ecocardiográfica extendida de los tres vasos (tres vasos y ductus), donde se muestra como una continuación recta del tronco pulmonar que se une a la trayectoria de la aorta descendente frente a la columna vertebral (Figura 2A). Una ligera angulación del transductor permite observar juntos el DA y el arco transverso, que forman una V en la región posterior del tórax, con el tronco pulmonar y el DA, como su brazo largo, y el arco aórtico transversal, como su brazo corto (Figura 2B).
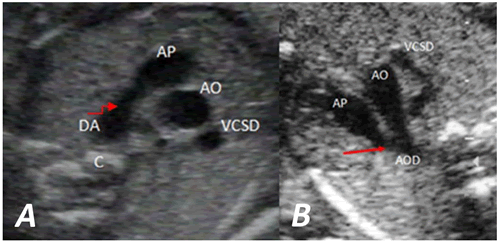
Figura 2. A. Vista ecocardiográfica extendida de los tres vasos (tres vasos y ductus) que muestra el ductus arteriosus como una continuación recta del tronco pulmonar que se une a la trayectoria de la aorta descendente frente a la columna vertebral. B. Una leve angulación del transductor permite observar juntos el conducto arterioso y el arco transverso que forman una V en la región posterior del tórax, con el tronco pulmonar y el DA, como su brazo largo, y el arco aórtico transversal, como su brazo corto. AP: arteria pulmonar, AO: aorta, AOD: aorta descendente, DA: ductus arterioso, C: columna vertebral, VCSD: vena cava superior derecha. Las flechas señalan el ductus arteriosus.
Corte angulado: se aprecia la vista del eje largo del ventrículo derecho donde se aprecia la arteria pulmonar que sale del ventrículo derecho y su continuación con el DA que finaliza en la aorta descendente (Figura 3).
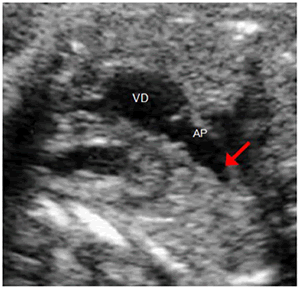
Figura 3. Vista ecocardiográfica del eje largo del ventrículo derecho donde se aprecia la arteria pulmonar que sale del mencionado ventrículo y a continuación el ductus arterioso (flecha), que finaliza en la aorta descendente. VD: ventrículo derecho AP: arteria pulmonar.
Corte longitudinal: mostrará el denominado arco ductal donde se aprecia la arteria pulmonar que sale del ventrículo derecho y su continuación con la aorta descendente (Figura 4).

Figura 4. Corte longitudinal del ductus denominado arco ductal (en un paciente con comunicación interventricular), donde se aprecia la arteria pulmonar saliendo del ventrículo derecho y su continuación con la aorta descendente. Entre ambas se señaliza el ductus arteriosus. AO: aorta. AOD: aorta descendente. TAP: tronco arteria pulmonar.
HEMODINÁMICA Y ANATOMÍA FETALES
El flujo del DA se dirige en condiciones normales siempre hacia la columna vertebral.
Existen varias referencias de alteraciones del DA, como su ausencia en la agenesia de válvulas pulmonares, o la presencia de un DA pequeño y tortuoso en posición anormal, como se aprecia en algunos casos de tetralogía de Fallot con atresia pulmonar y ramas no confluentes. La tortuosidad también es vista a medida que avanza la edad gestacional, la que además se hace menos recta. Se ha apreciado por algunos autores como Allan y colaboradores10 al final del embarazo un conducto ductal dilatado bulboso, que da la apariencia de un quiste en la parte inferior izquierda del tórax, pero se ha visto como una estructura normal que involuciona después del nacimiento.
El flujo invertido en el DA confirma una obstrucción grave del tracto de salida del ventrículo derecho10.
Si bien se conoce que existe un balance entre la vasoconstricción y la vasorelajación, y que, por lo tanto, la preponderancia de uno sobre el otro es la causa del cierre o la persistencia del vaso, actualmente se conocen mejor los factores que mantienen al conducto permeable durante la gestación, lo que, en realidad, genera que el análisis se centre en las vías de relajación muscular del vaso, y en sus posibles fallas.
La persistencia del ductus abierto durante la vida fetal es secundario a dos factores fundamentales:
La presión elevada en la luz del ductus, debido a la constricción del lecho pulmonar, debido (entre otras causas) al mecanismo de vasoconstricción hipóxica (propio de los vasos pulmonares) ocasionada por una baja presión alveolar de oxígeno16.
La producción basal de vasodilatadores [prostaglandinas (PG) y óxido nítrico]: La acción de las prostaglandinas vasodilatadoras E1, I2, E2. La I2 es la más abundante, pero la E2 es la más importante para mantener el ductus abierto, pues su potencia vasodilatadora ductal es 400 a 1000 veces mayor que la E1 y mucho más potente que la I2. Parecería ser que su origen es placentario. Normalmente el principal sitio de metabolización de las prostaglandinas es el lecho vascular pulmonar. Por lo tanto, debido a que en el feto la circulación a través del lecho pulmonar se ve reducida, se produce un desbalance fisiológico entre la producción placentaria de PGE2 y su metabolismo, lo que favorece los niveles altos de esta molécula. Esto es importante desde el punto de vista práctico, ya que contraindica el uso de inhibidores de las prostaglandinas, principalmente al final del embarazo. El óxido nítrico es producido por el propio ductus, y parecería jugar un rol importante en etapas tempranas de la gestación17.
MECANISMOS DE CIERRE
El cierre del conducto arterioso ocurre en dos fases; una de tipo funcional, que ocurre en las primeras horas luego del nacimiento y se debe a la vasoconstricción generada por la musculatura lisa del propio ductus. En los recién nacidos a término el cierre funcional del conducto ocurre en un 50 % a las 24 horas, en un 90 % a las 48 y en un 100 % a las 72 horas. Estos sucesos están favorecidos por diferentes mecanismos16,17:
– El aumento de la presión arterial de O2: el citocromo P450 (localizado en las células musculares del conducto) actuaría como el disparador de los acontecimientos inducidos por el oxígeno, los cuales consisten en el cierre de canales de K+, llamados oxígeno-sensibles, que generan una despolarización de la membrana celular. La cantidad de estos canales y su sensibilidad hacia el oxígeno varían entre las distintas especies, e incluso en distintos momentos de la gestación.
– Aumento de la formación de endotelina (potente vasoconstrictor).
– La disminución de la presión dentro de la luz del conducto, debido a la disminución de la resistencia vascular pulmonar.
– La caída de los niveles plasmáticos de PGE2, por la pérdida del tejido placentario y el aumento de la circulación pulmonar (prácticamente todo el caudal eyectado por el corazón).
– La disminución de la expresión de receptores de PGE2.
– La expresión (por parte de los miocitos) de isoformas de miosina con mayor capacidad contráctil, a medida que avanza la gestación.
La segunda fase de cierre es la de tipo anatómico. Ocurre luego de varios días, debido a la producción de ácido hialurónico por parte de las células endoteliales (las cuales, a su vez, comienzan a proliferar), lo que provee un ambiente favorable para la migración de las células musculares de la capa media, todo lo cual produce un engrosamiento progresivo de la túnica íntima17-20. Por otro lado, la contracción de los miocitos genera una isquemia en la capa media, debido a la oclusión de la vasa vasorum, lo cual induce la apoptosis de las células musculares, que consecuentemente adelgaza la túnica media. Una vez iniciada la contricción del ductus por alguno o varios de los mecanismos mencionados, hay un estacionamiento de la sangre, con lo cual se altera la nutrición de la pared del ductus (la que esencialmente ocurre desde el interior del vaso); ello lleva a que ocurra degeneración isquémica, necrosis de la pared y cambios citolíticos. Posteriormente ocurre proliferación de fibroblastos que lleva a que el ductus se convierta en el ligamento arterioso17.
El DA es una estructura noble y muy importante, debido a tres elementos fundamentales: resulta esencial en la vida fetal, permite ser manipulado farmacológicamente y puede existir como una cardiopatía, de ahí la necesidad de que los especialistas relacionados con esta rama de la medicina profundicen sus conocimientos sobre el tema.
Referencias bibliográficas
Schneider DJ, Moore JW. Patent ductus arteriosus. Circulation. 2006;114:1873-82.
Galen C. De usu partium corporis humani. In: Kühn CG, ed. Opera omnia, Medicorum Graecorum opera quae exstant. Leipzig: Georg Olms Verlagsbuchhandlung Hildesheim; 1964. p. 241-6.
May MT. Galen: On the usefulness of the parts of the body (Translated from the Greek). Ithaca, NY: Cornell University Press; 1968. p. 670-1.
Novack GJ, Rehman I. The ductus arteriosus in the human fetus and newborn infant. Anat Rec. 1941;81:505-27.
Harvey W. Exercitatio anatomica de motu cordis et sanguinis in animalisbus (Anatomical studies of the motion of the heart and blood). An English translation with annotations by Chauncey D Leake. 5ta ed. Riverwoods, IL: Springfield; 1978.
Marquis RM. The continuous murmur of persistence of the ductus arteriosus – An historical review. Eur Heart J. 1980;1:465-78.
Concepción M, Góngora D. Embriología cardiovascular. En: Díaz-Góngora G, Sandoval-Reyes N, Vélez-Moreno JF, Carrillo-Angel G, eds. Cardiología Pediátrica. Bogotá: McGraw-Hill Interamericana; 2003. p. 22-40.
Somoza F, Bruno M. Embriología cardiaca En: Somoza F, Bruno M, eds. Cardiología Pediátrica. Cardiología Perinatal. Buenos Aires: ISAG Bs. As.; 2007. p. 11-28.
García C, Savío A, García C, Somoza F, Arencibia J, Marantz P. Diagnóstico prenatal de anillo vascular con arco aórtico derecho. Rev Argent Cardiol. 2012;80:253-6.
Allan LD, Cook AC, Huggon IC. Fetal Echocardiography. A Practical Guide. Cambidge: University Press; 2009.
García C, Bernal Y, Hernández Y, Savío A, Díaz F, García C. Diagnóstico prenatal de doble arco aórtico. CorSalud [Internet]. 2013 [citado 26 Oct 2014];5:384-7. Disponible en: http://www.corsalud.sld.cu/sumario/2013/v5n4a13/doblearco.html
Allan L. Technique of fetal echocardiography. Pediatr Cardiol. 2004;25:223-33.
García C, Savío A, García C, Marantz P, San Luis R, Cazzaniga M, Somoza F. Vistas ecocardiográficas que no deben faltar durante la pesquisa de cardiopatías congénitas en el feto. Rev Fed Arg Cardiol [Internet]. 2013 [citado 30 Oct 2014];42(4):[aprox. 13 p.]. Disponible en: http://www.fac.org.ar/1/revista/13v42n4/art_revis/revis01/guevara.php
Viñals F. Visión de 3 vasos: Puesta al día. Rev Chil Ultrason. 2010;13:8-15.
Allan L. The normal fetal heart. En: Allan L, Hornberger L, Sharland G, eds. Textbook of Fetal Cardiology. London: Greenwich Medical Media; 2000. p. 55-95.
West J. Fisiología respiratoria. 7ma ed. Buenos Aires: Editorial Médica Panamericana; 2005. p. 141-57.
Clyman RI. Mechanisms regulating closure of the ductus arteriosus. En: Polin RA, Fox WW, Abman SH. Fetal and neonatal physiology. 4ta Ed. Philadelphia: Elsevier Saunders; 2011. p. 821-6.
Carlson B. Embriología humana y biología del desarrollo. 4ta ed. Barcelona: Elsevier España SL; 2009. p. 437-84.
Moore KL, Persaud TV. Embriología clínica. 8va ed. Barcelona: Elsevier España; 2008. p. 285-337.
Valdés A, Pérez HM, García RE, López A, García B, Matos JL, et al. Embriología humana. La Habana: Editorial Ciencias Médicas; 2010. p. 181-212
Recibido: 02 de noviembre de 2014
Aceptado: 09 de diciembre de 2014
Subir