CorSalud 2015 Abr-Jun;7(2):106-116
ARTÍCULO ORIGINAL
DISPERSIÓN DEL QRS COMO ÍNDICE DE DISINCRONÍA EN EL BLOQUEO DE RAMA IZQUIERDA Y DE SINCRONÍA TRAS LA TERAPIA DE RESINCRONIZACIÓN CARDÍACA, UNA VARIABLE DE RESPUESTA EXITOSA
Dr. CM. Elibet Chávez Gonzáleza,*, Dr. Alain Alonso Herrerab,*, Prof. Raimundo Carmona Puertaa,*, Dr. Damián Pérez Cabrerac, MSc. Dr. Ramiro R. Ramos Ramíreza,*, Dr. Walker Gómez Paimad, Dr. Francisco L. Moreno-Martíneze,*
______________
Servicio de Electrofisiología Cardíaca y Estimulación.
Unidad de Cuidados intensivos Posquirúrgicos.
Departamento de Ecocardiografía. Hospital Universitario "Arnaldo Milián Castro". Villa Clara, Cuba.
Servicio de Cardiología. Hospital Universitario "Celestino Hernández Robau". Villa Clara, Cuba.
Unidad de Hemodinámica y Cardiología Intervencionista.
* Cardiocentro "Ernesto Che Guevara". Villa Clara, Cuba.
Correspondencia: E Chávez González. Calle 1ra N° 18, e/ Unión y Río. Reparto Ramón Ruiz del Sol. Santa Clara, Villa Clara, Cuba. Correo electrónico: elibet@capiro.vcl.sld.cu
Resumen
Introducción: En pacientes con insuficiencia cardíaca, el bloqueo de rama izquierda del haz de His constituye un importante marcador de mal pronóstico, en ellos la terapia de resincronización puede mejorar la función del ventrículo izquierdo. Objetivo: Describir variables electrocardiográficas asociadas a una mejor respuesta de la resincronización cardíaca. Método: Se estudiaron 19 pacientes, 7 mujeres y 12 hombres con bloqueo de rama izquierda y fracción de eyección ≤ 35 %. Se realizó electrocardiograma antes y después de la terapia de resincronización, medición del QRS en las doce derivaciones y cálculo de su dispersión, se midieron voltajes máximos del QRS, y se realizaron ecocardiografías antes y después del procedimiento. Resultados: La fracción de eyección se incrementó desde 29,8±4,7 hasta 41,2±10,7 % (p=0.000). La correlación lineal entre fracción de eyección y dispersión del QRS a los seis meses de seguimiento fue significativa (r=0.34 y p=0.02); las mujeres presentaron mayor dispersión del QRS (48,0±24,0 vs. 37,14±13,8 ms; p=0.04). Los voltajes del QRS fueron predominantemente negativos en aVR (-0,52±0,58 vs. 0,28±0,42 mvolt; p=0.032) y positivos en V5 (0,71±1,12 vs. -0,15±1,20 mvolt; p=0.023) para los respondedores en relación con los no respondedores. Conclusiones: La dispersión del QRS incrementada en el electrocardiograma con bloqueo de rama izquierda y la disminución de la dispersión del QRS posresincronización demostraron correlaciones significativas con la fracción de eyección; además, el estrechamiento del QRS tras la resincronización fue significativo para los respondedores. Los voltajes predominantemente positivos en aVR y negativos en V5, pudieran predecir cuáles pacientes no responderán adecuadamente a la terapia de resincronización cardíaca.
Palabras clave: Terapia de resincronización cardíaca, Electrocardiograma, Insuficiencia cardíaca, Bloqueo de rama izquierda, Índice de disincronía eléctrica, Ventrículo izquierdo
QRS dispersion as an index of dyssynchrony in left bundle branch block and of synchrony after cardiac resynchronization therapy: A variable of successful response
Abstract
Introduction: Left bundle branch block is an important marker of poor prognosis in patients with heart failure. Resynchronization therapy can improve the function of the left ventricle in these cases. Objective: To describe electrocardiographic variables associated with a better response to cardiac resynchronization. Method: A total of 19 patients, 7 women and 12 men, with left bundle branch block and ejection fraction ≤ 35% were studied. An electrocardiogram was performed before and after resynchronization therapy, with QRS measurement in the twelve leads and calculation of its dispersion. Maximum QRS voltages were also measured. An echocardiogram was performed before and after the procedure. Results: The ejection fraction increased from 29.8±4.7 to 41.2±10.7 % (p=0.000). The linear correlation between ejection fraction and QRS dispersion at six months of follow-up was significant (r=0.34 and p=0.02). Women showed a greater QRS dispersion (48.0±24.0 ms vs. 37.14±13.8 ms; p=0.04). QRS voltages were predominantly negative in aVR (-0.52±0.58 vs. 0.28±0.42 mVolt; p=0.032) and positive in V5 (0.71±1.12 vs. -0.15±1.20 mVolt; p=0.023) for responders in relation to non-responders. Conclusions: QRS dispersion, increased in the electrocardiogram with left bundle branch block and decreased after resynchronization, showed a significant correlation with the ejection fraction. QRS narrowing after resynchronization was significant for responders. The predominantly positive voltages in aVR and negative in V5 could adequately predict which patients will not respond adequately to cardiac resynchronization therapy.
Key words: Cardiac resynchronization therapy, Electrocardiogram, Heart failure, Left bundle branch block, Electrical dyssynchrony index, Left ventricle
Introducción
La insuficiencia cardíaca crónica (ICC) continúa siendo un reto para la cardiología, su prevalencia en Estados Unidos, se estima alrededor de 2,4 % en adultos. A pesar del tratamiento médico óptimo, su hospitalización por descompensación y la muerte continúan siendo elevadas en los cinco primeros años del diagnóstico1. En los pacientes con ICC, los trastornos de conducción intraventricular constituyen un poderoso marcador de mal pronóstico, particularmente el bloqueo de rama izquierda del Haz de His (BRIHH)2-4.
La asincronía cardíaca es compleja y multifacética. La prolongación del intervalo atrio-ventricular (AV) retrasa la contracción sistólica, que podría dar lugar al llenado diastólico precoz. La presión auricular cae cuando las aurículas se relajan. Si la contracción ventricular se retrasa, las presiones diastólicas del ventrículo izquierdo (VI) exceden la presión auricular y se produce insuficiencia mitral diastólica. La pérdida de la precarga ventricular lleva entonces a una reducción de la contractilidad del VI, por la pérdida del mecanismo de Starling. El retraso de las conducciones inter e intraventricular causan contracción asincrónica entre regiones de la pared del VI (asincronía ventricular), lo que perjudica la eficacia cardíaca y reduce el volumen latido y la presión arterial sistólica. La función del músculo papilar mal coordinada puede causar o agravar la insuficiencia mitral sistólica funcional y un rendimiento deteriorado promueve el remodelado del VI5.
La terapia de resincronización cardíaca (TRC) ayuda a restaurar la sincronización AV, inter e intraventricular, con lo que mejora la función del VI, se reduce la insuficiencia mitral funcional y se induce remodelado inverso del VI, evidenciado por aumentos del tiempo de llenado del VI y su fracción de eyección (FEVI) y disminuciones de los volúmenes diastólicos y sistólicos finales del VI, de la insuficiencia mitral y la discinesia septal. El mecanismo dominante del beneficio probablemente varíe de un paciente a otro y en un mismo paciente con el paso del tiempo. Es posible que ninguna medición por sí sola diagnostique con exactitud la respuesta a la TRC, ya que los mecanismos del beneficio son muy heterogéneos5.
Los estudios MADIT-CRT y RAFT, han demostrado la utilidad de la TRC en pacientes con ICC y BRIHH4,6.
La búsqueda de parámetros clínicos, electrocardiográficos, ecocardiográficos y valores programables como los intervalos AV e interventriculares (VV) de los dispositivos de TRC han centrado la atención de los electrofisiólogos desde los inicios de esta terapia eléctrica para encontrar el candidato ideal de ser respondedor a la TRC8-12.
A pesar de estos esfuerzos, del 20 al 40 % de los pacientes que reciben un dispositivo para TRC, continúan mostrando una respuesta no favorable a esta forma de tratamiento13.
En el Cardiocentro Ernesto Che Guevara se comienza la implantación de dispositivos para TRC a inicios de 2010, donde se implantan aproximadamente entre 6 a 10 dispositivos por año, siempre a partir de los criterios de los expertos y las guías para la selección de los pacientes. Criterios que han cambiado a medida que han aparecido los resultados de los diferentes estudios que hasta el momento se han mencionado. En nuestra institución, se implanta un promedio de 15 a 20 dispositivos por millón de habitantes. El objetivo de esta investigación es describir resultados preliminares de variables electrocardiográficas asociadas a una mejor respuesta a la TRC.
Método
Se realizó un estudio prospectivo con 19 pacientes, de un total de 23, que recibieron un dispositivo para TRC en el Cardiocentro Ernesto Che Guevara de Santa Clara, Cuba, entre enero de 2010 y junio de 2014. El período mínimo de seguimiento fue de 11 meses. Las variables incluidas en el estudio pertenecen a los seis meses iniciales.
Este estudio fue aprobado por el Comité de Ética y el Consejo Científico del centro antes mencionado.
Criterios de inclusión
Pacientes con bloqueo de rama izquierda y QRS > 120 milisegundos (ms) y ritmo sinusal.
FEVI ≤ 35 %.
No evidencias de hipertensión pulmonar, descartada por ecocardiografía.
Arterias coronarias epicárdicas angiográficamente sin lesiones ateroscleróticas.
No evidencias clínicas al interrogatorio de cardiopatía isquémica.
Electrodo de seno coronario colocado en la vena lateral izquierda.
Clase funcional II-IV según la Asociación del Corazón de Nueva York (NYHA, por sus siglas en inglés), con tratamiento ambulatorio.
Ausencia de respuesta al tratamiento farmacológico óptimo.
Seguimiento y exclusión
Los pacientes fueron atendidos en consulta externa a la semana, al mes y a los tres y seis meses de implantado el dispositivo. De los 23 pacientes se excluyeron 4 por las siguientes causas:
- TRC con fibrilación atrial crónica y cardiopatía isquémica demostrada: 1
- Muerte por descompensación cardíaca: 1
- Electrodo del VI no ubicado en la vena lateral: 2
Ecocardiograma
Se consideraron inicialmente los criterios clásicos de la ecocardiografía para la inclusión de los pacientes según las guías 200714. En el 2010 se realizó una actualización de la mencionada guía y la ecocardiografía pasó a un segundo plano, de ahí que fuera de interés la FEVI calculada por los métodos de Simpson y de área-longitud. También se estimaron las presiones del tronco de la arteria pulmonar15 y se calcularon la FEVI, el diámetro telediastólico del VI y su volumen telesistólico antes de la implantación del dispositivo de TRC y a los seis meses después de implantado; variables útiles para clasificar a los pacientes en respondedores o no a la TRC.
Electrocardiograma (ECG)
ECG con BRIHH y duración del QRS > 120 ms para la clase funcional III-IV de la NYHA y QRS > 150 ms para los pacientes con clase II de la NYHA, según la actualización de las guías 2010, que fue cuando se inició el estudio15. Se realizó medición manual del QRS en las 12 derivaciones del ECG, registradas al unísono, estandarizado donde 10 milímetros (mm) equivalen a 1 milivoltio y la velocidad del papel fue de 25 mm/segundo. El QRS se midió desde la deflexión inicial de la onda hasta su terminación en el punto J, se calculó la diferencia de medida del QRS más ancho (QRSa) menos el QRS más estrecho (QRSe) y se obtuvo la variable dispersión del QRS (dQRS).
Fórmula: dQRS = QRSa - QRSe
Inmediatamente después de la implantación se programaron los siguientes parámetros en el dispositivo: VV sincrónico y retraso (delay) AV entre 100 y 120 ms, esto último en dependencia de la conducción AV con BRIHH. Si la conducción AV con BRIHH era igual o inferior a 130 ms, se programaba a 100 ms; si era superior a 130 ms, se programaba 120 ms. Una vez programados estos dos parámetros, se realizó ECG donde se calculó la dQRS.
Se midió, en las doce derivaciones, el mayor de los voltajes del QRS, desde su inicio en la línea basal hasta la cúspide de la R o el nadir de la S.
Selección de pacientes respondedores y no respondedores
Se consideraron respondedores aquellos pacientes con decremento > 15 % del volumen telesistólico del VI, un incremento de 5 % de la FEVI y mejoría de la clase funcional comprobado con la caminata de los 6 minutos. Los pacientes que no alcanzaron los valores mencionados se consideraron no respondedores.
Análisis estadístico
Se utilizó una base de datos creada en el paquete estadístico SPSS v.17.0 para Windows. Se comprobó la distribución normal de la muestra y se obtuvo p>0.05 para la prueba Shapiro-Wilk, lo que nos permitió realizar otros pruebas paramétricas. Se realizó distribución de frecuencia de las variables numéricas en estudio y comparaciones de medias y regresión lineal para comprobar la existencia de asociación estadística: significativo (p≤0.05), altamente significativo (p≤0.001) y no significativo (p≥0.05).
Resultados
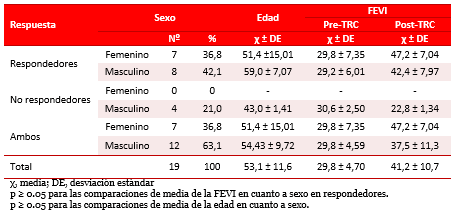
Se estudiaron 12 hombres y 7 mujeres (Tabla 1). Todas las mujeres estudiadas fueron respondedoras a la TRC y solo 4 hombres (21 %) fueron no respondedores. La media de la FEVI previa a la TRC fue similar para ambos sexos y para los grupos de respondedores o no, entre 29,2 y 30,6 %. El incremento, en cuanto a la media, de la FEVI en los respondedores fue discretamente superior en el grupo de las mujeres (47,2 vs. 42,4 %) sin mostrar diferencias significativas (p=0.262). El grupo de no respondedores mostró una caída para la media de la FEVI. El incremento de esta variable para toda la muestra fue desde 29,8±4,70 % hasta 41,2±10,7 %, p=0.000.
Tabla 1. Distribución de los pacientes según sexo, media para la edad, respuesta a la TRC y media de la FEVI antes y seis meses después de la implantación del dispositivo.
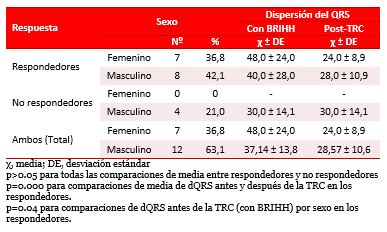
La dQRS, (Tabla 2) con BRIHH, mostró un valor superior en los respondedores de sexo femenino comparado con los masculinos (40,0±28,0 vs. 48,0±24,0 ms); sin embargo, no mostró diferencias significativas (p>0.05). Inmediatamente después de implantado y reprogramado el dispositivo, según se explicó en el método, se realizó ECG y se calculó la dQRS; obsérvese que el decremento de la dQRS en los hombres respondedores fue de 28,0±10,9 ms y en las mujeres, 24,0±8,9 ms (p=0.234). Las comparaciones de media de la dQRS, con BRIHH y posresincronización, respecto al sexo (hombres 40,0±28,0 vs. 28,0±10,9 ms y mujeres 48,0±24,0 vs. 24,0±8,9 ms) mostraron diferencias significativas (p=0.000). La comparación de media de la dQRS para el total de la muestra estudiada fue de 37,14±13,8 vs. 48,0±24,0 ms, en masculinos y femeninos, respectivamente; lo que demuestra diferencias significativas (p=0.04). En el grupo de los no respondedores este valor de dQRS (30,0±14,1 ms) no varió.
Tabla 2. Distribución de la media para la dispersión del QRS previo e inmediatamente después de la implantación, según la respuesta a la TRC.
Una correlación lineal, para el grupo de los respondedores, entre la FEVI a los seis meses de seguimiento (Gráfico 1), como variable dependiente y la dQRS con BRIHH como independiente mostró un coeficiente de correlación r=0.34 y p=0.02. La misma prueba estadística fue aplicada para los respondedores entre la FEVI a los seis meses de seguimiento y la dQRS en el ECG después de la TRC (Gráfico 2), y se constató que a medida que decrecía la dQRS se incrementaba la FEVI (r= -0.40 y p=0.000).
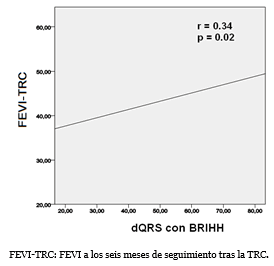
Grafico 1. Correlación lineal entre la FEVI y la dQRS en el ECG con BRIHH.
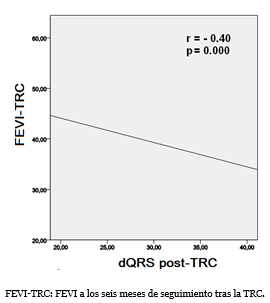
Grafico 2. Correlación lineal entre la FEVI y la dQRS en el ECG postimplante del dispositivo.
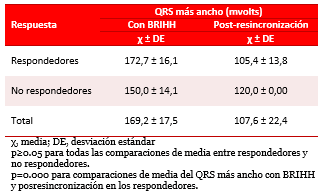
La distribución de los valores de media para los QRS más anchos medidos con BRIHH e inmediatamente después de la TRC se muestra en la tabla 3. El grupo de los respondedores presentó una media del QRS más ancho superior a la de los no respondedores (172,7±16,1 vs. 150±14,1 ms), sin existir diferencias significativas (p>0.05). Una vez implantado el dispositivo, el QRS se estrechó en los respondedores desde 172,7±16,1 hasta 105±13,8 ms (p=0.000). El decremento en la media del ancho del QRS para los no respondedores fue de hasta 120 ms, sin demostrar diferencias significativas (p>0.05).
Tabla 3. Distribución de los valores de media para los QRS más anchos medidos con BRIHH e inmediatamente después de la resincronización.
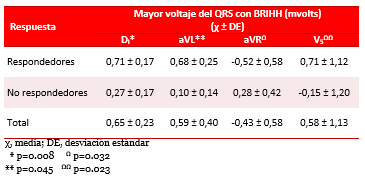
El voltaje del QRS en las doce derivaciones permitió identificar diferencias en algunas de ellas (DI, aVL, aVR, V5) según el grupo de pacientes (respondedores o no) (Tabla 4). Los respondedores mostraron mayores voltajes de la onda R en DI que los no respondedores (0,71±0,17 vs. 0,27±0,17 mvolt; p=0.008), así sucedió también para el voltaje de la R en aVL (0,68±0,25 vs. 0,10±0,14 mvolt; p=0.045). El voltaje del QRS en aVR en los respondedores fue predominantemente negativo, comparado con los no respondedores en quienes fue positivo (-0,52±0,58 vs. 0,28±0,42 mvolt; p=0.032). Para V5 la media del QRS fue positivo, con R de 0,71±1,12 mvolt, al compararlo con los no respondedores donde predominaron las negatividades del QRS (-0,15±1,20 mvolt; p=0.023).
Tabla 4. Distribución de los valores de media para los mayores voltajes del QRS en algunas derivaciones del ECG, según respuesta a la TRC.
Discusión
El 100 % de las mujeres seleccionadas para nuestro estudio fueron respondedoras a la TRC, la Guía de Práctica Clínica de la Sociedad Europea de Cardiología de 2013 sobre estimulación y terapia de resincronización cardíacas, al explicar las posibilidades de mejor respuesta a la TRC, mencionan que los criterios expuestos en la guía representan la visión mayoritaria del grupo de trabajo, pero no todos los que contribuyeron estaban de acuerdo. Varias declaraciones se basan en el análisis por subgrupos de ensayos clínicos aleatorizados, lo que plantea muchos problemas de interpretación (interrelación entre morfología y duración del QRS, diferencias por sexo en la respuesta, beneficio diagnóstico en pacientes isquémicos o no isquémico) o con áreas de incertidumbre que aún son objeto de estudio (papel potencial de la asincronía ecocardiográfica en el QRS estrecho). Y terminan diciendo que futuros estudios podrían cambiar el conocimiento y las recomendaciones5.
A nuestro entender relacionan un grupo de criterios que demuestran que existe heterogeneidad en la selección de las muestras en los estudios de TRC. Para este estudio, en función de homogeneizar la muestra (véase criterios de inclusión), se estudiaron 19 pacientes sin clínica referida de cardiopatía isquémica, con arterias epicárdicas sin lesiones angiográficas y con el electrodo del VI colocado en la vena lateral. Sin embargo, a pesar de este intento de homogeneizar, el grupo de mujeres estudiadas en su totalidad respondió a la TRC; mientras que solo lo hizo el 66 % de los hombres. Ellas representaron el 36,8 % del total de la muestra.
Xu y colaboradores16, mencionan en su estudio, que coincide con los resultados porcentuales del nuestro, que el porcentaje de mujeres estudiadas con TRC ha sido siempre inferior en la mayoría de las investigaciones; además, plantean que ambos géneros tienen igual respuesta significativa a la TRC al referirse al incremento de la FEVI. Esto último también coincide con nuestros resultados, pues a pesar de que las mujeres tuvieron mayor FEVI que los hombres respondedores (47,2 vs. 42,4 %), no existieron diferencias significativas. Sin embargo, Varma et al.17, demostraron diferencias de género al describir que con un QRS > 150 ms respondieron a la TRC el 86 % de las mujeres vs. 36 % de los hombre y con QRS < 150 ms 83 vs. 69 %, respectivamente. Loring et al.18, plantean que la mejor respuesta a la TRC de las mujeres respecto a los hombres puede deberse a un mayor número de falsos positivos al seleccionar los BRIHH en el sexo masculino y no a diferencias de otras variables ya estudiadas.
No se encontró ningún informe en la literatura revisada1-48 que mencione el estudio de la dQRS. Al reflexionar en cuanto a la teoría existente sobre la dispersión de la onda P del ECG39-41, que explica las diferencias regionales en los tiempos de activación atrial por trastornos de la conducción intra e interatrial, se piensa que en presencia de BRIHH, donde se han demostrado retrasos eléctricos de algunas zonas del corazón –por ejemplo de la pared lateral del VI con respecto al septum interventricular5,18–, también podrían encontrarse valores máximos y mínimos de duración del QRS que permitieran calcular su dispersión, por lo cual se decidió estudiar esta nueva variable.
La observación preliminar que podemos mencionar es la mayor dQRS en el sexo femenino (100 % respondedoras a la TRC), al igual que el decremento de esta dQRS, al comparar los ECG antes (con BRIHH) e inmediatamente después la TRC, que fue más marcado en las mujeres; además de las correlaciones significativas de la FEVI en el ecocardiograma de seguimiento con la dQRS. Se podría estar entonces en presencia de una nueva variable a evaluar en posteriores estudios, la dQRS, la cual demostró en nuestra investigación, que la mayor dQRS en el ECG con BRIHH (antes de la TRC) y la mayor regresión de ese valor de dispersión tras la TRC, se relacionan mayores incrementos de la FEVI y mejoría de la clase funcional. En otras palabras pudiera decirse que la dQRS puede convertirse en una excelente variable para predecir el resultado de la TRC.
Se propone denominar a la dQRS: índice de disincronía eléctrica del VI en presencia de bloqueo de rama izquierda. Los resultados preliminares que aquí se exponen demuestran la existencia de mayor dQRS en pacientes con los QRS más anchos en presencia de BRIHH y se ha comprobado la existencia de mayor disincronía eléctrica en pacientes con QRS > 150 ms5,17,18; aspecto este muy bien señalado por Varma42 en 2009, al demostrar retrasos en la activación del ventrículo izquierdo. Además, la regresión de la dQRS, es mayor en los que responden favorablemente a la TRC, lo que puede estar asociado al restablecimiento de la sincronía eléctrica y tendría que demostrarse desde el punto de vista electrofisiológico. Se observó además que las derivaciones más anchas fueron DI y aVL, resultados no mostrados en este artículo, que serán objeto de posterior publicación.
El ancho del QRS siempre ha sido cuestión de interés para seleccionar los respondedores o no a la TRC, en las guías de actuación5,14,15 se menciona el beneficio de este tratamiento en los pacientes con BRIHH > 150 ms5,38. Se ha considerado que un QRS inferior a 130 ms puede predecir una mala respuesta a la TRC43.
Dupont et al.44, señalan la importancia de la morfología y duración del QRS para obtener una mejor respuesta a la TRC, ellos consideraron como punto de corte 150 ms, aunque es justo señalar que en su trabajo los pacientes con BRIHH y QRS > 150 ms, tuvieron un incremento de la FEVI de 12±12 % y en aquellos con QRS < 150 ms el incremento de la FEVI fue de 8±10 %; por lo tanto, como el incremento de la FEVI fue mayor a 5 % en ambos grupos, deben considerarse los dos como respondedores, aunque los autores encontraron diferencias significativas entre estos valores (p<0.05). Sin embargo, Guglin y Curtis45, han planteado que es lógico esperar que a mayor duración del QRS mejor será la respuesta del paciente a la TRC, pues es mayor la disincronía eléctrica entre el septum y la pared lateral del VI. Ellos mencionan además que los estudios actuales han demostrado incrementos de la FEVI de 28,4±7,3 % a 33,9±9,7 % (p<0.001) en pacientes con QRS entre 120 y 150 ms, y de 26,0±12,9 % a 37,0±12,5 % (p<0.001), en pacientes con QRS > 150ms, lo que demuestra que en estos dos grupos el incremento de la FEVI fue de aproximadamente 5,5±7,3 % vs. 11,0±12,1 % (p=0.04), por lo que no se puede negar la posibilidad de que los pacientes con BRIHH y QRS entre 120-150 ms pueden ser buenos respondedores a la TRC. Por esta razón sugieren continuar estudiando estas diferencias o, sencillamente, dividir los grupos en incrementos pequeños de la FEVI y considerar finalmente que 150 ms no es un número mágico en la decisión de seleccionar un paciente para la TRC. La reducción inicial del ancho del QRS tras la TRC, se ha registrado en el estudio REVERSE como un criterio de buena respuesta a este tipo de terapia eléctrica46. Nuestros resultados coinciden con estos planteamientos, pues se encontró que en los pacientes respondedores disminuyó significativamente la anchura del QRS (decremento de la media de 67 ms), mientras que los no respondedores tuvieron una reducción de solo 30 ms.
La morfología del QRS, también está relacionada con la buena respuesta a la TRC46,47, los pacientes con franco BRIHH que reúnen los criterios para este trastorno de conducción intraventricular, han demostrado ser los de mejor respuesta a la TRC. Al igual que se ha mencionado que los pacientes con BRIHH, sin desviación axial del eje del QRS a la derecha o a la izquierda, son mejores respondedores10.
Nuestros resultados demuestran que los pacientes respondedores tienen voltajes dentro de la normalidad en las derivaciones de los planos frontal y horizontal [DI, aVL, aVR, V5 (Tabla 4)]. No se objetivaron las desviaciones del eje eléctrico del QRS, solo se realizó la observación de que en los respondedores existe una tendencia a presentar voltajes normales en las mencionadas derivaciones. Los no respondedores presentaron menores voltajes positivos en las derivaciones del plano frontal (DI y aVL) y voltajes predominantemente positivos en aVR y negativos en V5, esto último denotó una pobre progresión ascendente del voltaje de la R en las derivaciones precordiales (hasta V5) en los no respondedores.
García-Seara et al.48, observaron que los pacientes con BRIHH y desviación axial izquierda del eje eléctrico, a los cuales se les colocaba el electrodo de VI en la vena lateral, tenían una mejor respuesta a la TRC; sin embargo, Brenyo et al.10, demostraron que la mejor respuesta a la TRC estaba en los pacientes con BRIHH sin desviación axial izquierda del eje del QRS. Loring et al.18, concluyeron que las diferencias encontradas en la respuesta a la TRC entre mujeres y hombres no está asociada a la comorbilidad, pues demostraron que los no respondedores no contaban con un ECG con criterios reales de BRIHH, sino que tenían patrones electrocardiográficos similares que podían estar justificados por demoras de la conducción intraventricular izquierda. Quizás las diferencias encontradas en los voltajes del QRS para los no respondedores, en las derivaciones estudiadas de nuestra muestra, estén relacionadas con otro tipo de trastorno de conducción intraventricular izquierdo y no un verdadero BRIHH.
En adición a lo anterior, Josephson y Wellens49, en Josephson Wellens ECG Lessons: A monthly visit to the 12 lead ECG han planteado que la presencia de una R terminal positiva en aVR y predominio negativo en V5 (R/S < 1) se asocia a crecimiento o afectación de ventrículo derecho, mencionan además que si estos hallazgos son crónicos pueden predecir una pobre respuesta a la TRC.
Conclusiones
El ECG continúa siendo una herramienta útil al seleccionar a los pacientes para TRC. La mayor dQRS en el ECG con BRIHH tuvo una asociación significativa con el incremento de la FEVI a los seis meses de seguimiento tras la TRC. La reducción significativa de la dQRS tras la TRC demostró correlación significativa con el aumento de la FEVI en el seguimiento. Las mujeres presentaron mayores valores de dQRS en el ECG con BRIHH y demostraron ser las de mejor respuesta a la TRC. El estrechamiento del QRS, que coincide con la reducción de la dQRS, tras la TRC fue significativa en los respondedores. Los pacientes con voltajes predominantemente positivos en aVR y negativos en V5 no respondieron adecuadamente a la TRC, observación que puede ser útil al seleccionar a los pacientes para este tipo de tratamiento. La dQRS pudiera ser una variable útil para predecir la respuesta a la TRC.
Limitaciones del estudio
Se trata de un estudio con una muestra pequeña, con implantación del electrodo de VI en la vena lateral, y donde no se aplicaron pruebas funcionales de gran valor, como la tomografía por emisión de fotón único o la resonancia magnética nuclear, para descartar la presencia de cardiopatía isquémica; por lo que su ausencia fue solo definida por la clínica y la coronariografía. Por ello los resultados aquí obtenidos necesitan ser reproducidos y evaluados en muestras con diferentes características y comorbilidades. Además, no se evalúan otras variables electro y ecocardiográficas ampliamente difundidas en la literatura revisada. Por último, no haber comprobado la posible relación entre QRS más ancho/dispersión del QRS/disincronía eléctrica del VI.
Referencias bibliográficas
Roger VL, Go AS, Lloyd-Jones DM, Adams RJ, Berry JD, Brown TM, et al. Heart disease and stroke statistics – 2011 update: A report from the American Heart Association. Circulation. 2011;123:e18-e209.
Linde C, Abraham WT, Gold MR, St John Sutton M, Ghio S, Daubert C, et al. Randomized trial of cardiac resynchronization in mildly symptomatic heart failure patients and in asymptomatic patients with left ventricular dysfunction and previous heart failure symptoms. J Am Coll Cardiol. 2008;52:1834-43.
Moss AJ, Hall WJ, Cannom DS, Klein H, Brown MW, Daubert JP, et al. Cardiac-resynchronization therapy for the prevention of heart-failure events. N Engl J Med. 2009;361:1329-38.
Tang AS, Wells GA, Talajic M, Arnold MO, Sheldon R, Connolly S, et al. Cardiac-resynchronization therapy for mild-to-moderate heart failure. N Engl J Med. 2010;363:2385-95.
Brignole M, Auricchio A, Barón-Esquivias G, Bordachar P, Boriani G, Breithardt OA, et al. Guía de práctica clínica de la ESC 2013 sobre estimulación cardiaca y terapia de resincronización cardiaca. Rev Esp Cardiol. 2014;67:58.e1-e60.
Zareba W, Klein H, Cygankiewicz I, Hall WJ, McNitt S, Brown M, et al. Effectiveness of cardiac resynchronization therapy by QRS morphology in the multicenter automatic defibrillator implantation trial-cardiac resynchronization therapy (MADIT-CRT). Circulation. 2011;123:1061-72.
Cuoco FA, Gold MR. Optimization of cardiac resynchronization therapy: Importance of programmed parameters. J Cardiovasc Electrophysiol. 2012;23:110-8.
Holmqvist F, Daubert JP. More bad news for cardiac resynchronization therapy in atrial fibrillation patients: What to do? J Cardiovasc Electrophysiol. 2013;24:1123-4.
Sebag FA, Martins RP, Defaye P, Hidden-Lucet F, Mabo P, Daubert JC, et al. Reverse electrical remodeling by cardiac resynchronization therapy: Prevalence and clinical impact. J Cardiovasc Electrophysiol. 2012;23:1219-27.
Brenyo A, Rao M, Barsheshet A, Cannom D, Quesada A, McNitt S, et al. QRS axis and the benefit of cardiac resynchronization therapy in patients with mildly symptomatic heart failure enrolled in MADIT-CRT. J Cardiovasc Electrophysiol. 2013;24:442-8.
Cochet H, Denis A, Ploux S, Lumens J, Amraoui S, Derval N, et al. Pre- and intra-procedural predictors of reverse remodeling after cardiac resynchronization therapy: An MRI Study. J Cardiovasc Electrophysiol. 2013;24:682-91.
Arbelo E, Tolosana JM, Trucco E, Penela D, Borràs R, Doltra A, et al. Fusion-optimized intervals (FOI): a new method to achieve the narrowest QRS for optimization of the AV and VV intervals in patients undergoing cardiac resynchronization therapy. J Cardiovasc Electrophysiol. 2014;25:283-92.
Abraham WT, Fisher WG, Smith AL, Delurgio DB, Leon AR, Loh E, et al. Cardiac resynchronization in chronic heart failure. N Engl J Med. 2002;346:1845-53.
Vardas PE, Auricchio A, Blanc JJ, Daubert JC, Drexler H, Ector H, et al. Guidelines for cardiac pacing and cardiac resynchronization therapy: The Task Force for Cardiac Pacing and Cardiac Resynchronization Therapy of the European Society of Cardiology. Developed in collaboration with the European Heart Rhythm Association. Eur Heart J. 2007;28:2256-95.
Dickstein K, Vardas PE, Auricchio A, Daubert JC, Linde C, McMurray J, et al. 2010 focused update of ESC Guidelines on device therapy in heart failure: An update of the 2008 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure and the 2007 ESC Guidelines for cardiac and resynchronization therapy. Developed with the special contribution of the Heart Failure Association and the European Heart Rhythm Association. Eur Heart J. 2010;31:2677-87.
Xu YZ, Friedman PA, Webster T, Brooke K, Hodge DO, Wiste HJ, et al. Cardiac resynchronization therapy: Do women benefit more than men? J Cardiovasc Electrophysiol. 2012;23:172-8.
Varma N, Manne M, Nguyen D, He J, Niebauer M, Tchou P. Probability and magnitude of response to cardiac resynchronization therapy according to QRS duration and gender in nonischemic cardiomyopathy and LBBB. Heart Rhythm. 2014;11:1139-47.
Loring Z, Caños DA, Selzman K, Herz ND, Silverman H, MaCurdy TE, et al. Left bundle branch block predicts better survival in women than men receiving cardiac resynchronization therapy: long-term follow-up of ∼ 145,000 patients. JACC Heart Fail. 2013;1:237-44.
Ford J, Sears S, Ramza B, Reynolds DW, Nguyen P, Fedewa M, et al. The Registry Evaluating Functional Outcomes of Resynchronization Management (REFORM): Quality of life and psychological functioning in patients receiving cardiac resynchronization therapy. J Cardiovasc Electrophysiol. 2014;25:43-51.
Lindsay BD. Perspective on cost-effective utilization of cardiac resynchronization therapy. J Cardiovasc Electrophysiol. 2013;24:75-6.
Hayat SA, Kojodjojo P, Mason A, Benfield A, Wright I, Whinnett Z, et al. Malfunction of subpectorally implanted cardiac resynchronization therapy defibrillators due to weakened header bond. J Cardiovasc Electrophysiol. 2013;24:351-5.
Doguet F, Honoré C, Godin B, Anselme F. Isolation of the phrenic nerve to suppress diaphragmatic contraction induced by cardiac resynchronization. J Cardiovasc Electrophysiol. 2012;23:778-80.
D´Onofrio A, Botto G, Mantica M, La Rosa C, Occhetta E, Verlato R, et al. Incremental value of larger interventricular conduction time in improving cardiac resynchronization therapy outcome in patients with different QRS duration. J Cardiovasc Electrophysiol. 2014;25:500-6.
Lenarczyk R, Kowalski O, Sredniawa B, Pruszkowska-Skrzep P, Mazurek M, Jędrzejczyk-Patej E, et al. Implantation feasibility, procedure-related adverse events and lead performance during 1-year follow-up in patients undergoing triple-site cardiac resynchronization therapy: A substudy of TRUST CRT randomized trial. J Cardiovasc Electrophysiol. 2012;23:1228-36.
Derval N, Bordachar P, Lim HS, Sacher F, Ploux S, Laborderie J, et al. Impact of pacing site on QRS duration and its relationship to hemodynamic response in cardiac resynchronization therapy for congestive heart failure. J Cardiovasc Electrophysiol. 2014;25:1012-20.
Bose A, Kandala J, Upadhyay GA, Riedl L, Ahmado I, Padmanabhan R, et al. Impact of myocardial viability and left ventricular lead location on clinical outcome in cardiac resynchronization therapy recipients with ischemic cardiomyopathy. J Cardiovasc Electrophysiol. 2014;25:507-13.
van Boven N, Bogaard K, Ruiter J, Kimman G, Theuns D, Kardys I, et al. Functional response to cardiac resynchronization therapy is associated with improved clinical outcome and absence of appropriate shocks. J Cardiovasc Electrophysiol. 2013;24:316-22.
Kandala J, Upadhyay GA, Altman RK, Bose A, Heist EK, Mela T, et al. Electrical delay in apically positioned left ventricular leads and clinical outcome after cardiac resynchronization therapy. J Cardiovasc Electrophysiol. 2013;24:182-7.
Gold MR, Leman RB, Wold N, Sturdivant JL, Yu Y. The effect of left ventricular electrical delay on the acute hemodynamic response with cardiac resynchronization therapy. J Cardiovasc Electrophysiol. 2014;25:624-30.
Bogaard MD, Hesselink T, Meine M, Loh P, Hauer RN, Cramer MJ, et al. The ECG in cardiac resynchronization therapy: influence of left and right ventricular preactivation and relation to acute response. J Cardiovasc Electrophysiol. 2012;23:1237-45.
Ploux S, Verdoux H, Whinnett Z, Ritter P, Dos Santos P, Picard F, et al. Depression and severe heart failure: Benefits of cardiac resynchronization therapy. J Cardiovasc Electrophysiol. 2012;23:631-6.
Noyes K, Veazie P, Hall WJ, Zhao H, Buttaccio A, Thevenet-Morrison K, et al. Cost-effectiveness of cardiac resynchronization therapy in the MADIT-CRT trial. J Cardiovasc Electrophysiol. 2013;24:66-74.
Huizar JF, Kaszala K, Koneru JN, Thacker LR, Ellenbogen KA. Comparison of different pacing strategies to minimize phrenic nerve stimulation in cardiac resynchronization therapy. J Cardiovasc Electrophysiol. 2013;24:1008-14.
Rickard J, Cheng A, Spragg D, Cantillon D, Baranowski B, Varma N, et al. A clinical prediction rule to identify patients at heightened risk for early demise following cardiac resynchronization therapy. J Cardiovasc Electrophysiol. 2014;25:278-82.
Weinstock J, Estes NA. Cardiac resynchronization therapy: extending current responses to phrenic nerve stimulation. J Cardiovasc Electrophysiol. 2014;25:491-3.
Ortega M, Merino JL, Blanco FV, Gutiérrez-Larraya F. Cardiac resynchronization therapy in an infant with double outlet right ventricle and mechanical dyssynchrony. J Cardiovasc Electrophysiol. 2012;23:781-3.
van Boven N, Theuns D, Bogaard K, Ruiter J, Kimman G, Berman L, et al. Atrial fibrillation in cardiac resynchronization therapy with a defibrillator: a risk factor for mortality, appropriate and inappropriate shocks. J Cardiovasc Electrophysiol. 2013;24:1116-22.
Stavrakis S, Lazzara R, Thadani U. The benefit of cardiac resynchronization therapy and QRS duration: A meta-analysis. J Cardiovasc Electrophysiol. 2012;23:163-8.
Dilaveris PE, Gialafos JE. P-wave dispersion: A novel predictor of paroxysmal atrial fibrillation. Ann Noninvasive Electrocardiol. 2001;6:159-65.
Chávez E, Carmona R. Dispersión de la onda P, uso del método manual de medición como recomendación para la práctica médica. Experiencia del Cardiocentro "Ernesto Che Guevara". CorSalud [Internet]. 2011 [citado 30 Ene 2015];3:303-9. Disponible en: http://www.corsalud.sld.cu/sumario/2011/v3n4a11/dispersion.htm
Chávez E, González E, Llanes MC, Garí M, García J, Fernández E, et al. Dispersión de la onda P en niños hipertensos, su relación con el peso corporal. CorSalud [Internet]. 2012 [citado 30 Ene 2015];4:272-7. Disponible en: http://www.corsalud.sld.cu/sumario/2012/v4n4a12/ondap.html
Varma N. Left ventricular conduction delays and relation to QRS configuration in patients with left ventricular dysfunction. Am J Cardiol. 2009;103:1578-85.
Ruschitzka F, Abraham WT, Singh JP, Bax JJ, Borer JS, Brugada J, et al. Cardiac-resynchronization therapy in heart failure with a narrow QRS complex. N Engl J Med. 2013;369:1395-405.
Dupont M, Rickard J, Baranowski B, Varma N, Dresing T, Gabi A, et al. Differential response to cardiac resynchronization therapy and clinical outcomes according to QRS morphology and QRS duration. J Am Coll Cardiol. 2012;60:592-8.
Guglin M, Curtis. AB. QRS duration criteria to select patients for cardiac resynchronization therapy: Cardiac resynchronization therapy: 150 is not a magic number!. Circ Arrhythm Electrophysiol. 2013;6:429-35.
Gold MR, Thébault C, Linde C, Abraham WT, Gerritse B, Ghio S, et al. Effect of QRS duration and morphology on cardiac resynchronization therapy outcomes in mild heart failure: results from the Resynchronization Reverses Remodeling in Systolic Left Ventricular Dysfunction (REVERSE) study. Circulation. 2012;126(7):822-9.
Al Hebaishi YS, Al Shehri HZ, Al Moghairi AM. Predictors of cardiac resynchronization therapy response: The pivotal role of electrocardiogram. ScientificWorldJournal [Internet]. 2013 [citado 05 Feb 2015];2013:837086[aprox. 6 p.]. Disponible en: http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3615583/pdf/TSWJ2013-837086.pdf
García-Seara J, Martínez-Sande JL, Cid B, Gude F, Bastos M, Domínguez M, et al. Influencia del eje eléctrico QRS preimplante en la respuesta a la terapia de resincronización cardiaca. Rev Esp Cardiol. 2008;61:1245-52.
Josephson ME, Wellens HJ. The ECG in left bundle branch block and heart failure. Heart Rhythm. 2015;12:250-1.
Recibido: 12 de febrero de 2015
Aceptado: 19 de marzo de 2015
Subir