CorSalud 2012 Jul-Sep;4(3):151-156
ARTÍCULO ORIGINAL
PROFILAXIS DE LA NEFROPATÍA INDUCIDA POR CONTRASTE EN PACIENTES DE ALTO RIESGO CON SÍNDROME CORONARIO AGUDO SIN ELEVACIÓN DEL SEGMENTO ST
Dr. Pablo Revilla Martí*, Dr. Jose A. Linares Vicente**, Dra. Antonela Lukic**, Dra. Pilar Artero Bello*, Dr. Ramón Bascompte Claret*, Dra. Tatiana Matajira Chia*, Dra. Pilar Portero Pérez** y Dr. Jose R. Ruiz Arroyo**
______________
* Servicio de Cardiología.
** Unidad de Cardiología Intervencionista.
Hospital Clínico Universitario "Lozano Blesa". Zaragoza, España.
Resumen
Introducción y objetivos: La eficacia de la administración conjunta de suero salino isotónico y N-acetilcisteína presenta resultados dispares en la prevención de la nefropatía por contraste yodado. Nuestro objetivo fue valorar la posible eficacia de esta estrategia combinada en pacientes con alto riesgo de desarrollar nefropatía inducida por contraste, ingresados y sometidos a intervencionismo coronario percutáneo por síndrome coronario agudo sin elevación del segmento ST en nuestro centro. Método: Se aplicó esta estrategia en los pacientes referidos, con al menos un factor de alto riesgo para desarrollar la nefropatía inducida por contraste: mayores de 80 años, diabetes mellitus, creatinina basal mayor de 1,5 mg/dl o alto volumen de contraste (mayor de 400 ml). El protocolo se aplicó durante 12 meses (pacientes que recibieron el protocolo de prevención) y se comparó con similares pacientes en los 12 meses previos que no recibieron profilaxis. Resultados: Un total de 30 pacientes (24 %) desarrollaron nefropatía inducida por contraste. El porcentaje fue significativamente mayor en el grupo que no recibió profilaxis: 35,9 % vs. 11,5 % (p = 0.003). Conclusiones: La combinación de N-acetilcisteína por vía oral e hidratación parenteral en pacientes de alto riesgo, con síndrome coronario agudo sin elevación de ST, podría ser beneficiosa para evitar la aparición de la nefropatía inducida por contraste.
Palabras clave: Intervencionismo coronario, contraste yodado, nefropatía por contraste
Abstract
Introduction and Objectives: The effectiveness of the administration of isotonic saline solution and N-acetylcysteine shows different results in the prevention of iodine contrast nephropathy. Our objective was to assess the potential effectiveness of this combined strategy in patients at high risk for contrast-induced nephropathy, who were admitted in our center for percutaneous coronary intervention due to non-ST-segment elevation acute coronary syndrome. Method: This strategy was applied in the patients mentioned, with at least one risk factor for developing contrast-induced nephropathy: over 80 years, diabetes mellitus, baseline creatinine greater than 1.5 mg / dl or high volume of contrast (greater than 400 ml). The protocol was applied for 12 months (patients that received the prevention protocol) and compared with similar patients in the previous 12 months who received no prophylaxis. Results: A total of 30 patients (24 %) developed contrast-induced nephropathy. The percentage was significantly higher in the group that did not receive prophylaxis: 35.9 % vs. 11.5 % (p = 0.003). Conclusions: The combination of N-acetylcysteine orally and parenteral hydration in high-risk patients with acute coronary syndrome without ST elevation could be beneficial to avoid the appearance of contrast-induced nephropathy.
Key words: Coronary intervention, iodine contrast medium, contrast-induced nephropathy
Introducción
El empleo de contrastes yodados para la realización de técnicas diagnósticas y terapéuticas cardiovasculares se ha incrementado a lo largo de las últimas décadas. Actualmente la nefropatía inducida por contraste (NIC) constituye la tercera causa de insuficiencia renal aguda intrahospitalaria, y aunque en la mayoría de los casos es de carácter leve con gradual recuperación posterior, llega a presentar una mortalidad del 14 %. La incidencia de la NIC en la población general oscila entre 0,6 - 2,3 %; sin embargo, en pacientes de alto riesgo la incidencia puede llegar a ser hasta del 50 %, según recientes estudios1,2. En este grupo se encuentran los pacientes que presentan alguna de las siguientes características: mayores de 75 años, insuficiencia renal previa, antecedente de diabetes mellitus, anemia o insuficiencia cardíaca, o las relativas al intervencionismo (empleo de volúmenes elevados de contraste, hipotensión mantenida o empleo de balón de contrapulsación)3-5.
Se han estudiado diferentes medidas preventivas con el objetivo de evitar la aparición de esta complicación. La hidratación adecuada periprocedimiento ha demostrado consistentemente su eficacia. El empleo de N-acetilcisteína presenta en la literatura resultados contradictorios6-8, y recientemente un largo ensayo clínico ha demostrado ausencia de beneficio clínico9. Sin embargo, el posible beneficio del uso combinado de estas dos medidas (hidratación junto con administración de N-acetilcisteína), especialmente en pacientes de muy alto riesgo, no está suficientemente demostrado en la literatura.
Nuestro objetivo no ha sido otro que valorar la posible eficacia de esta estrategia combinada en pacientes con alto riesgo de desarrollar NIC, ingresados y sometidos a intervencionismo coronario percutáneo (ICP) por síndrome coronario agudo sin elevación del segmento ST (SCASEST) en el Hospital Clínico Universitario "Lozano Blesa" de Zaragoza, España.
Método
Durante los años 2010-2011 se introdujo, como proyecto de mejora de calidad asistencial, la aplicación de un protocolo de prevención de la NIC tras cateterismo cardíaco, consistente en la administración de 1000 ml de suero fisiológico en 12 horas periprocedimiento y 1200 mg/12h de N-acetilcisteína por vía oral, durante 2 días. El estudio se llevó a cabo a lo largo de 2 años: durante el año de implantación del protocolo de profilaxis se recogieron los datos de forma prospectiva, y se compararon con una recogida retrospectiva del año previo a la aplicación de dicho protocolo.
Se incluyeron a todos los pacientes ingresados en la Unidad Coronaria del Hospital Clínico Universitario de Zaragoza con diagnóstico SCASEST, a los que se les realizó cateterismo cardíaco en el plazo de 24-48 horas y presentaban, al menos, uno de los siguientes factores de alto riesgo para el desarrollo de NIC: edad mayor de 80 años, creatinina basal mayor de 1,5 mg/dl, antecedente de diabetes mellitus o empleo de más de 400 ml de contraste durante el ICP. Se excluyeron los pacientes que requirieron uso de inotropos endovenosos, balón de contrapulsación intraaórtico o ventilación mecánica, así como los que presentaban oligoanuria o anuria en las 24 horas previas al procedimiento, o estaban en programa de diálisis.
De la historia clínica se obtuvieron los datos referentes a edad, sexo, antecedentes de hipertensión arterial, dislipidemia, diabetes mellitus y tabaquismo, y cifras máximas de creatin-fosfoquinasa (CK) y troponina I. De la base de datos de la sección de Cardiología Intervencionista se recogieron el número de vasos con enfermedad coronaria grave, el número de lesiones tratadas así como el volumen de contraste administrado.
Los parámetros de laboratorio (cifras de creatinina y su aclaramiento) fueron determinados a la llegada del paciente al hospital y a las 48 horas posteriores a la realización del cateterismo cardíaco. El aclaramiento de creatinina se estimó mediante la fórmula de Cockcroft-Gault.
En todos los casos el contraste angiográfico utilizado fue iobitridol; medio de contraste hidrosoluble, no iónico y de baja osmolaridad.
Se dividió a los pacientes en dos grupos en función de la aplicación del protocolo de administración de la profilaxis de la NIC. El objetivo primario del estudio fue la aparición de nefropatía inducida por contraste, que se definió como un aumento de la cifra de creatinina de 0,5 mg/dl o del 25 %, respecto a la creatinina basal, a las 48 horas del procedimiento.
El análisis estadístico se realizó con el programa SPSS 19. Las variables continuas se expresaron como media ± desviación estándar y las cualitativas como porcentajes. Las variables continuas que siguen una distribución normal, según la prueba de Kolmogorov-Smirnov, se analizaron utilizando la "t de Student" para muestras independientes. Las variables binarias y categóricas, se analizaron mediante la prueba de Chi-cuadrado y ANOVA, respectivamente. El nivel de significación estadístico alfa se estableció en 0.05. La razón de riesgo se calculó con un intervalo de confianza del 95 % y el número de pacientes necesarios a tratar se calculó, según el inverso del riesgo absoluto.
Resultados
Durante 24 meses se incluyeron en el estudio 125 pacientes: 61 en el grupo de protocolo de profilaxis (N-acetilcísteina junto con hidratación con suero fisiológico), y 64 fuera del protocolo, recogidos durante los 12 meses previos a su aplicación.
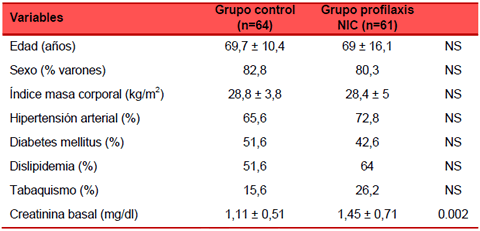
La tabla 1 muestra las características basales de los dos grupos, con similares características epidemiológicas. Los valores de creatinina basal fueron mayores en el grupo sometido al protocolo (1,11 ± 0,51 mg/dl vs. 1,45 ± 0,71 mg/dl).
Tabla 1. Características basales.
En la tabla 2 se recogen las características del intervencionismo coronario en cada grupo: la densidad y distribución de la enfermedad coronaria, y su tratamiento fue similar en ambos grupos, si bien el tamaño del infarto fue discretamente superior en los pacientes no sometidos a la profilaxis (TnI: 19,8 ± 17,6 ng/ml vs. 13,9 ± 14,4 ng/ml, p = 0.04). Es destacable un mayor aumento de la creatinina después del procedimiento en los pacientes que no recibieron profilaxis frente a los que la recibieron (0,36 ± 0,68 mg/dl vs. 0,11 ± 0,69 mg/dl; p = 0.05).
Tabla 2. Características del procedimiento.
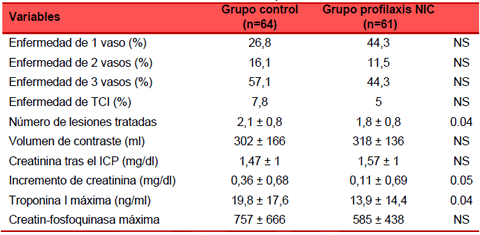
NS: No significativa.
TCI: Tronco común izquierdo
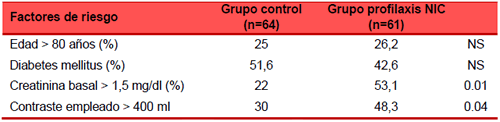
La tabla 3 refleja el resumen de las indicaciones de profilaxis de NIC, donde se muestra un mayor porcentaje de pacientes sometidos a alto volumen de contraste en el grupo tratado (30 % vs. 48,3 %, p = 0.04).
Tabla 3. Indicación de profilaxis para la nefropatía inducida por contraste.
Un total de 30 pacientes (24 %) desarrollaron NIC. El porcentaje de NIC fue significativamente mayor en el grupo que no recibió profilaxis de la NIC: 35,9 % (23/64) vs. 11,5 % (7/61) (p = 0.003), lo que se comportó como un factor protector para su aparición con un riesgo relativo de 0,32 (IC 95 % 0,15 a 0,69). El número de pacientes necesarios a tratar para evitar una NIC fue de 4 (IC 95 % 3 a 10).
Discusión
En nuestro centro la aplicación del protocolo de hidratación junto con N-acetilcisteína en pacientes con SCASEST con alto riesgo de desarrollar NIC, resultó eficaz para disminuir su incidencia. Se decidió utilizar altas dosis de N-acetilcisteína ya que previamente se había constatado la superioridad de la dosis de 1200 mg frente a la de 600 mg, dos veces al día10.
Muchos estudios han valorado la capacidad de la N-acetilcisteína para prevenir la NIC. En el trabajo de Tepel et al.11 y el estudio APART12, la administración profiláctica de N-acetilcisteína junto con la hidratación parenteral, fue superior a la hidratación aislada para prevenir la NIC en pacientes con creatinina sérica basal elevada (2 % vs. 21 % y 8 % vs. 45 %, respectivamente).
Recientemente varios estudios han presentado resultados similares13-15. Sin embargo, podemos encontrar diversos trabajos discordantes. Briguori et al.16 no consiguieron demostrar el beneficio de la N-acetilcisteína junto con la hidratación frente a la hidratación exclusivamente en 183 pacientes. Del mismo modo, la administración intravenosa de N-acetilcisteína en 487 pacientes con alteración de la función renal tampoco resultó eficaz a la hora de prevenir la NIC en el estudio de Webb et al.17 Se han atribuido varios factores a esta disparidad de resultados, pero la heterogeneidad en la metodología de los estudios se considera el principal de ellos. Muchos estudios incluían sólo pacientes con insuficiencia renal, sin otros factores de riesgo entre los descritos para el desarrollo de NIC. El estudio ACT, multicéntrico, aleatorizado y controlado con placebo, tampoco consiguió demostrar el papel protector de la N-acetilcisteína9. Se incluyeron 2308 pacientes con al menos un factor de riesgo para el desarrollo de NIC y se aleatorizaron a altas dosis de N-acetilcisteína 1200 mg (dos veces al día) antes y después del procedimiento o placebo. La incidencia de NIC resultó similar en ambos grupos 12,7 % (p = 0.97). Los límites que definieron para los pacientes con riesgo fueron la edad mayor a 70 años (menor que en nuestra muestra) y el volumen de contraste mayor a 140 ml, mucho menor que el elegido y posiblemente más alejado de la realidad del tratamiento de la enfermedad coronaria multivaso en un solo procedimiento.
La hipótesis de esta investigación sugiere que la ausencia de beneficio descrita en algunos trabajos podría ser debida a la falta de pacientes de alto riesgo en los grupos tratados, de manera que si el beneficio existiera solamente en éstos, se diluiría en número total de pacientes. Razón por la cual se decidió analizar los datos procedentes de los pacientes de muy alto riesgo. De igual manera se evaluaron los que presentaron SCASEST, pues son de alto riesgo por definición, ingresados en una unidad de cuidados intensivos, y que permitían el acceso a una analítica basal y posterior al procedimiento de forma homogénea. Los restrictivos criterios de alto riesgo (edad superior a 80 años, antecedente de diabetes mellitus, insuficiencia renal significativa o volumen de contraste administrado durante el procedimiento superior a 400 ml) determinaron una casuística menor que la esperada por la epidemiología del SCASEST, que no permitió una correcta aleatorización y que posiblemente sea la causa de las diferencias basales entre los 2 grupos. Sin embargo, este hecho apoya nuestra hipótesis, de manera tal que a pesar de que los pacientes que recibieron profilaxis presentaban un perfil inicial de mayor riesgo (mayor porcentaje de insuficiencia renal y volumen elevado de contraste), presentaron menor incidencia de NIC que el grupo control.
Conclusiones
Nuestro estudio muestra, con sus limitaciones por la escasa casuística, que en pacientes ingresados y sometidos a ICP por SCASEST con alto riesgo de desarrollar NIC, el empleo conjunto de hidratación parenteral con suero salino isotónico y N-acetilcisteína podría ser beneficiosa para su prevención.
Conflictos de intereses
Los autores expresan que no existían conflictos de intereses en el momento de redactar este manuscrito.
Referencias bibliográficas
Vercellino M, Bezante GP, Balbi M. Contrast medium induced nephropathy: new insights into prevention and risk management. Cardiovasc Hematol Agents Med Chem. 2009;7(2):166-80.
Chong E, Poh KK, Shen L, Chai P, Tan HC. Diabetic patients with normal baseline renal function are at increased risk of developing contrast-induced nephropathy post-percutaneous coronary intervention. Singapore Med J. 2009;50 (3):250-4.
Mehran R, Aymong ED, Nikolsky E, Lasic Z, Iakovou I, Fahy M, et al. A simple risk score prediction of contrast-induced nephropathy after percutaneous coronary intervention. J Am Coll Cardiol. 2004;44(7):1393-9.
Rihal CS, Textor SC, Grill DE, Berger PB, Ting HH, Best PJ, et al. Incidence and prognostic importance of acute renal failure after percutaneous coronary intervention. Circulation. 2002;105(19):2259-64.
Jian-hua LI, Neng-shu HE. Prevention of iodinated contrast-induced nephropathy. Chinese Medical Journal. 2011;124(23):4079-82.
Nallamoth BK, Shojania KG, Saint S, Hofer TP, Humes HD, Moscucci, et al. Is acetylcysteine effective in preventing contrast-related nephropathy? A meta-analysis. Am J Med. 2004;117(12):938-47.
Gonzales DA, Norsworthy KL, Kern SJ, Banks S, Slevng PC, Star RA, et al. A meta-analysis of N-acetylcysteinein contras-induced nephrotoxicity: unsupervised clustering to resolve heterogeneity. BMC Med. 2007;5:32.
Bagshaw SM, McAlister FA, Manns BJ, Ghali WA. Acetylcysteine in the prevention of contrast-induced nephropathy: a case study on the pitfalls in the evolution of evidence. Arch Intern Med. 2006;166:161-6.
ACT Investigators. Acetylcysteine for prevention of renal outcomes in patients undergoing coronary and peripheral vascular angiography: main results from the Randomized Acetylcysteine for Contrast-Induced Nephropathy Trial (ACT). Circulation. 2011;124(11):1250-9.
Trivedi H, Daram S, Szabo A, Bartorelli AL, Marenzi G. High dose N-acetylcisteine for the prevention of contrast induced nephropathy. Am J Med. 2009;122(9):874.e9-15.
Tepel M, van der Giet M, Schwarzfeld C, Laufer U, Liermann D, Zidek W. Prevention of radiographic-contrast-agent-induced reductions in renal function by acetylcysteine. N Engl J Med. 2000;343(3):180-4.
Díaz-Sandoval LJ, Kosowsky BD, Losordo DW. Acetylcysteine to prevent angiography-related renal tissue injury (the APART trial). Am J Cardiol. 2002;89(3):356-8.
Calabro P, Bianchi R, Crisci M, Caprile M, Bigazzi MC, Palmieri R, et al. Use and efficacy of saline hydratation and N- acetyl cysteine to prevent contrast-induced nephropathy in low-risk populations undergoing coronary artery angiography. Intern Emerg Med. 2011;6(6):503-7.
Koc F, Ozdemir K, Kaya MG, Dogdu O, Vatankulu MA, Ayhan S, et al. Intravenous N-acetylcysteine plus high-dose hydratation versus high-dose hydration and standard hydration for the prevention of contrast-induced nephropathy: CASIS- a multicenter prospective controlled trial. Int J Cardiol. 2012;155(3):418-23.
Marenzi G, Assanelli E, Marana I, Lauri G, Campodonico J, Grazi M, et al. N-acetylcysteine and contrast-induced nephropathy in primary angioplasty. N Engl J Med. 2006;354(26):2773-82.
Briguori C, Manganelli F, Scarpato P, Elia PP, Golia B, Riviezzo G, Lepore S, et al. Acetylcysteine and contrast agent-associated nephrotoxicity. J Am Coll Cardiol. 2002;40(2):298-303.
Webb JG, Pate GE, Humphries KH, Buller CE, Shalansky S, Al Shamari A, et al. A randomized controlled trial of intravenous N-acetylcysteine for the prevention of contrast-induced nephropathy after cardiac catheterization: lack of effect. Am Heart J. 2004;148(3):422-9.
Recibido: 1 de mayo de 2012
Aceptado para su publicación: 4 de junio de 2012