|
CorSalud 2012;4(2) |
ARTICULO ORIGINAL
FACTORES CLÍNICOS Y DEL PROCEDIMIENTO RELACIONADOS CON
Por:
Dr.
Guillermo Pacheco González1, Dr.C.
Ángel G. Obregón Santos2, Dr. Ronald Aroche Aportela3, Dr.C. Héctor Conde Cerdeira4, Dr. Myder Hernández
Navas5 y Dr. Julio C. Gandarilla Sarmientos6
______________
1.
Especialista
de I Grado en Cardiología y MGI. Hospital Militar Central “Dr. Luis Díaz Soto”.
2.
Doctor en Ciencias Médicas.
Especialista de II
Grado en Cardiología. Centro de
Investigaciones Médico-Quirúrgicas.
3.
Especialista
de II Grado en Cardiología y de I Grado en MGI. Centro de Investigaciones
Médico-Quirúrgicas.
4.
Doctor en Ciencias Médicas.
Especialista II Grado en Cardiología. Centro de Investigaciones Médico-Quirúrgicas.
5.
Especialista
de I Grado en Cardiología y MGI. Hospital General Docente “Enrique Cabrera”.
6.
Especialista
de I Grado en Cardiología y MGI. Instituto de Cardiología y Cirugía
Cardiovascular.
Resumen
Introducción y objetivos: La trombosis del stent es una de las complicaciones
posterior al intervencionismo coronario percutáneo, asociada a una
elevada mortalidad y morbilidad. A pesar del uso de la doble terapia
antiplaquetaria (aspirina y clopidogrel) y la optimización de la técnica, su
incidencia no ha desaparecido. El objetivo de esta investigación fue determinar
los factores de riesgo de trombosis de los stent
metálicos convencionales. Método: Se realizó un estudio
descriptivo-retrospectivo. De las 2.014 arterias revascularizadas en el Centro de
Investigaciones Médico-Quirúrgicas de
Abstract
Introduction and
Objectives: Stent thrombosis is a
complication after percutaneous coronary intervention associated with high
mortality and morbidity. Despite the use of dual antiplatelet therapy (aspirin
and clopidogrel) and optimization of the technique, its incidence has not
disappeared. The objective of this research was to determine the risk factors
for thrombosis of the bare metal stents. Method: A retrospective descriptive study was performed. Out of
the 2,014 revascularized arteries at the Medical-Surgical Research Center in
Havana, Cuba, between August 1997 and February 2009, the 289 redo ones were
selected. Results:
thrombosis of the conventional metal stents was present in 20 arteries, of
which 11 corresponded to the anterior descending artery, and the highest
incidence occurred in the first 24 hours and after 30 days. Diabetes mellitus
was a risk factor for thrombosis (OR = 3.06) and the release pressure of less
than 10 atmospheres (OR = 3.70) and complex lesions of types B2 and
C (OR = 8.80), all with statistical significance (p <0.05). Conclusions: The highest incidence of bare
metal stent thrombosis was on the first day of revascularization after the
termination of dual antiplatelet therapy and located in the anterior descending
artery. Diabetes mellitus, complex lesions and low pressures of stent release,
behaved as risk factors for thrombosis with statistically significant results.
|
Palabras clave: ENFERMEDAD CORONARIA ANGIOPLASTIA PRÓTESIS
VASCULAR TROMBOSIS FACTORES DE RIESGO |
Key words: CORONARY DISEASE ANGIOPLASTY BLOOD VESSEL
PROSTHESIS THROMBOSIS RISK FACTORS |
Nota del Editor: *OR (odds ratio): razón de
probabilidades o posibilidades, índice de probabilidades, cociente de
probabilidades. Hay quien plantea con frecuencia la conveniencia de no traducir
este término y aceptar directamente el anglicismo odds ratio (OR).
Introducción
Cuando se comenzaron a implantar los primeros stents (inicialmente el Gianturco-Roubin y el Palmaz-Schatz), que
hoy día llamamos convencionales (BMS,
por sus siglas en inglés), las indicaciones de su uso fueron fundamentalmente
de tipo anatómico y, por tanto, muy limitadas. Estas endoprótesis coronarias
lograron incrementar la seguridad de los procedimientos intervencionistas, como
lo demuestra el hecho de que con su uso se redujeron a 1 - 2 % las tasas de
oclusión aguda, que acontecían hasta en el 12 % de los casos; esta práctica se
asoció a la administración sistemática de los regímenes antiplaquetarios dobles.
Esto hizo que se superase la fase restrictiva de indicación clínica, en la que
los stents sólo se implantaban en
casos de oclusión o amenaza de oclusión de la arteria tratada1.
La trombosis del stent
(TS) es una de las complicaciones que ocurren posterior al intervencionismo
coronario percutáneo (ICP) y se asocian a una elevada morbilidad y
mortalidad. A pesar del uso de la doble terapia antiplaquetaria (aspirina y
clopidogrel) y de la optimización de la técnica, su incidencia no ha
desaparecido. Estos son nuevos problemas que surgen tras haber introducido
técnicas nuevas que aportan grandes beneficios. No es poner de manifiesto el
problema sino conocer sus causas y lograr soluciones para abolir, o al menos
minimizar, sus efectos negativos.
El objetivo de esta investigación fue determinar los factores de riesgo de trombosis de los stent metálicos convencionales.
Método
Se realizó un estudio descriptivo-longitudinal-retrospectivo
en pacientes intervenidos en el laboratorio de hemodinámica del Cardiocentro
del Centro de Investigaciones Médico-Quirúrgicas (CIMEQ) de
La información se obtuvo a partir de la
historia clínica, los informes de los procedimientos intervencionistas y la
base de datos en el programa ANGYCOR, donde se registra de forma continua la
actividad de cardiología intervencionista en formato digital y convencional. En
los casos en que fue necesario se acudió a la grabación del procedimiento en el
disco compacto, que permanece en el archivo de este laboratorio, para la
aclaración de alguna información. Los datos obtenidos se registraron en una
base de datos creada al efecto con el programa SPSS versión 15.0, con el cual
se analizó posteriormente la información.
Resultados
La trombosis de los BMS estuvo presente en 20
arterias, de las cuales 11 resultaron ser la descendente anterior (DA).
En
nuestro estudio la trombosis tuvo la mayor incidencia en dos momentos muy
importantes con relación a la doble terapia antiagregante plaquetaria: al
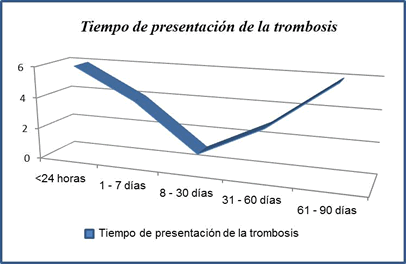
inicio y al final del tratamiento. En las primeras 24 horas posteriores al
procedimiento, la trombosis tuvo una incidencia de seis casos; sin embargo,
esta disminuye a partir del octavo día para volver a incrementarse a partir de
los 30 días, momento en que se suspende el clopidogrel (Gráfico 1).
|
Gráfico 1. Presentación de la
trombosis según los días posteriores al intervencionismo. |
Al
analizar las características clínicas basales de los pacientes de nuestra serie
en relación con la trombosis, se pudo determinar que la diabetes mellitus se
comportó como un factor de riesgo importante (OR = 3,06), y resultó
estadísticamente significativo, lo cual no ocurrió con el resto de las
variables estudiadas (Tabla 1).
Tabla 1. Características
clínicas y riesgo de trombosis.
Características |
Trombosis n(%) |
OR |
Intervalo Confianza |
p |
|
Masculino |
15
(1,3%) |
0,68 |
0,24-1,88 |
0,454 |
|
Hipertensión |
10
(1,4%) |
1,14 |
0,47-2,76 |
0,767 |
|
Diabetes mellitus |
6
(3,2%) |
3,06 |
1,16-8,07 |
0,017* |
|
Tabaquismo |
11
(1,4%) |
1,11 |
0,46-6,69 |
0,824 |
|
Dislipidemia |
6
(1,7%) |
1,39 |
0,53-3,62 |
0,502 |
|
Infarto previo |
12
(2,1%) |
1,06 |
0,38-2,62 |
0,350 |
|
Multiarteriales |
7
(2,1%) |
1,85 |
0,73-4,68 |
0,187 |
*Estadísticamente
significativo
Fuente:
Ficha de recolección de datos.
El
estudio de las características angiográficas y del procedimiento, en relación
con la trombosis, nos permite determinar como factores de riesgo de esta
complicación, la impactación del stent a
bajas presiones (menos de 10 atmósferas) y las lesiones complejas de los tipo B2
y C, con OR=3,7 y OR = 8,8; respectivamente (Tabla 2).
Tabla 2. Características
angiográficas y del procedimiento, y riesgo de
trombosis.
Características |
Trombosis n(%) |
OR |
Intervalo Confianza |
p |
|
Arteria < |
12(1,3%) |
1,97 |
0,80-4,85 |
0,131 |
|
Stent > 18mm |
18(1,1%) |
1,75 |
0,40-7,59 |
0,447 |
|
Oclusión total |
2(0,7%) |
0,62 |
0,15-2,82 |
0,562 |
|
DLM < 1mm |
15(1,1%) |
1,52 |
0,55-4,20 |
0,415 |
|
< 10 atmósferas |
9(2,4%) |
3,70 |
1,52-9,00 |
0,002* |
|
Lesiones B2 y C |
19(1,4%) |
8,8 |
1,17-65,85 |
0,010* |
|
Lesión en CD |
5(1,1%) |
1,09 |
0,39-3,01 |
0,872 |
|
Lesión en DA |
11(1,3%) |
1,74 |
0,72-4,22 |
0,213 |
|
Lesión en CX |
4(1,7%) |
1.86 |
0,62-5,62 |
0,262 |
*Estadísticamente
significativo
Fuente: Ficha de recolección de datos.
Discusión
La
trombosis de stent depende de cuatro
grupos de factores: relacionados con el stent,
el paciente, la lesión y con el procedimiento1-4.
En este estudio la
casuística de TS fue en los stents
metálicos convencionales, pues son estos los más utilizados. No hubo ningún
caso de trombosis de stents
liberadores de fármacos (SLF).
En
septiembre de 2006 la Administración de Alimentos y Fármacos (FDA,
por sus siglas en inglés) se vio obligada a realizar una declaración sobre la
seguridad de los SLF, en respuesta a la creciente preocupación sobre la
posibilidad de un aumento de la mortalidad, debido a la trombosis tardía del stent (TTS)5, fundamentalmente basado en los estudios BASKET-LATE6 y el metaanálisis de
Camenzind7, el primero
con un seguimiento de 18 meses y el segundo de 3 años, donde se pudo observar un
aumento significativo de los infartos de miocardio fatales y no fatales en el
grupo de los SLF5. La
publicación de Camenzind y colaboradores informó mayores efectos adversos con
el sirolimus7.
Otros estudios no
demostraron un aumento significativo de los sucesos cardiovasculares mayores
asociado a TTS, lo que hace a este tema controversial. Análisis recientes,
sugieren un incremento del riesgo
de trombosis del 0,5 % con los SLF9-10.
La fisiopatología de
En la declaración de
En
las características relacionadas con el paciente se reconocen como factores de
riesgo: la edad avanzada, la diabetes mellitus, la implantación del stent en el curso de un síndrome
coronario agudo, la presencia de una fracción de eyección baja y el abandono de
la doble terapia antiagregante.
En
este estudio, la utilización de stents
metálicos en los pacientes con diabetes mellitus
aumentó el riesgo de trombosis. Según la literatura consultada y los últimos
estudios publicados, se recomienda el uso de los SLF en este grupo de pacientes
diabéticos16.
La trombosis del BMS es más
frecuente que ocurra durante el primer mes posterior al intervencionismo. En esta serie se comportó
de igual manera, donde se identificaron dos momentos de mayor incidencia (las
primeras 24 horas y alrededor del día 30), relacionados con el inicio o la suspensión
de la doble terapia antiagregante17-18.
Está
demostrado que algunos pacientes, a pesar de cumplir un adecuado tratamiento
farmacológico de doble antiagregación plaquetaria, manifiestan resistencia a la
aspirina o al clopidogrel, y en la mayoría de los laboratorios no se realizan
análisis de rutina para determinar previamente los pacientes con resistencia a
la antiagregación19.
Determinadas
características de las lesiones se comportan como factores de riesgo, como son
las lesiones en bifurcación y las lesiones complejas, con lo cual coincidimos,
pues esta serie demuestra que las lesiones de los tipos B2 y C
elevan el riesgo en más de ocho veces con relación a las lesiones de tipo A.
Se
plantea que existen aspectos técnicos que pueden favorecer al desarrollo de la
trombosis del stent, por lo que se
hace necesaria la optimización del procedimiento. Se debe prestar especial atención
al lumen final pequeño, el flujo
coronario lento persistente y la implantación de múltiples stents. En esta serie se pudo identificar que la impactación del stent a bajas presiones (< 10 atmósferas),
eleva el riesgo de trombosis más de tres veces12,20.
Para
lograr un mejor resultado en la prevención de la trombosis de stents se hace necesaria una adecuada
optimización del procedimiento durante la angioplastia, por ello se debe de
incluir, si fuera necesario, la utilización del ultrasonido intravascular
posterior a la implantación del stent,
así como la aplicación de la técnica de doble globo (kissing balloon, en inglés)20
en las bifurcaciones, y una minuciosa inspección posterior al
procedimiento en busca de disecciones residuales.
Conclusiones
La mayor incidencia de trombosis de los stent metálicos convencionales fue en el
primer día de la revascularización, después de la terminación de la doble
terapia de antiagregación plaquetaria y en la arteria descendente anterior. La
diabetes mellitus, las lesiones complejas y las bajas presiones de liberación
del stent, se comportaron como
factores de riesgo de trombosis con resultados estadísticamente significativos.
Referencias
bibliográficas
1.
Balaguer-Malfagón
JR, Pomar-Domingo F, Vilar-Herrero JV, Planas-del Viejo AM, Pérez-Fernández E.
Trombosis del stent en la era
moderna: incidencia, consecuencias y factores predictores. Rev Esp Cardiol.
2006;59(8):842-5.
2. Cutlip DE, Baim DS, Ho KK, Popma JJ, Lansky AJ, Cohen DJ. Stent
Thrombosis in the Modern Era: A Pooled Analysis of Multicenter Coronary Stent
Clinical Trials. Circulation. 2001;103;1967-71.
3. Applegate RJ, Sacrinty MT, Kutcher MA, Santos RM, Gandhi SK, Baki TT, et al. “Off-label” stent therapy 2-year
comparison of drug-eluting versus bare-metal stents. J Am Coll Cardiol.
2008;51(6):607-14.
4.
Íñiguez Romo A.
Trombosis de los stents farmacoactivos.
Rev Esp
Cardiol. 2008;61(7):674-7.
5.
US Food and Drug Administration [sitio web en
Internet]. Silver Spring; 2006 [actualizado
21 Dic 2008]. Disponible en: http://www.fda.gov/ohrms/dockets/ac/cdrh06.html#circulatory
6. Pfisterer M, Brunner-La Rocca HP, Buser PT,
Rickenbacher P, Hunziker P, Mueller C, et
al. Late clinical events after clopidogrel discontinuation
may limit the benefit of drug-eluting stents: an observational study of
drug-eluting versus bare-metal stents. J Am Coll Cardiol. 2006;48(12):2584-91.
7. Camenzind E, Steg PG, Wijns W. Stent thrombosis late after implantation
of first-generation drug-eluting stents: a cause for concern. Circulation.
2007;115(11):1440-55.
8. Cutlip DE, Windecker S, Mehran R, Boam A, Cohen DJ, van Es GA, et al. Clinical end points in coronary
stent trials: a case for standardized definitions. Circulation.
2007;115(17):2344-51.
9. Mauri L, Hsieh WH, Massaro JM, Ho KK, D’Agostino R, Cutlip DE. Stent thrombosis in randomized clinical trials of drug-eluting stents. N Engl J Med. 2007;356:1020-9.
10. Daemen J, Wenaweser P, Tsuchida K, Abrecht L, Vaina
S, Morger C, et al. Early and late coronary stent thrombosis of sirolimus-eluting and
paclitaxel eluting stents in routine clinical practice: data from a large
two-institutional cohort study. Lancet. 2007;369 (9562):619-21.
11. Joner M, Finn AV, Farb A, Mont EK, Kolodgie FD,
Ladich E, et al. Pathology of drug-eluting stents in humans: delayed healing and late
thrombotic risk. J Am Coll Cardiol.
2006;48(1):193-202.
12. Bavry AA, Bhatt DL. Appropriate use of drug-eluting stents:
balancing the reduction in restenosis with the concern of late thrombosis. Lancet. 2008;371(9630):2134-43.
13. Jaffe R, Strauss BH. Late and very late thrombosis of drug-eluting
stents evolving concepts and perspectives. J Am Coll Cardiol. 2007;50 (2):119-27.
14. Spertus JA, Kettelkamp R, Vance C, Decker C, Jones
PG, Rumsfeld JS, et al. Prevalence, predictors, and outcomes of premature discontinuation of
thienopyridine therapy after drug-eluting stent placement: results from the
PREMIER registry. Circulation. 2006;113(24):2803-9.
15.
Eisenstein EL,
Anstrom KJ, Kong DF, Shaw LK, Tuttle RH, Mark DB, et al. Clopidogrel use and long-term
clinical outcomes after drug-eluting stent implantation. JAMA.
2007;297(2):159-68.
16.
Jiménez-
Quevedo P, Sabaté M, Angiolillo DJ, Alfonso F, Hernández-Antolín R,
Gómez-Hospital JA, et al. Eficacia de
la implantación del stent recubierto
de rapamicina en pacientes diabéticos con vasos muy pequeños (menor e igual a
17. Stettler C, Wandel S, Allemann S, Kastrati A, Morice MC, Schömig A, et al. Outcomes associated with
drug-eluting and bare-metal stents: a collaborative network meta-analysis.
Lancet. 2007;370(9591):937-48.
18. Doyle B, Rihal CS, O’Sullivan CJ, Lennon RJ, Wiste HJ, Bell M, et al. Outcomes of stent thrombosis and
restenosis during extended follow-up of patients treated with bare-metal
coronary stents. Circulation. 2007(21);116:2391-8.
19. Wiviott SD, Braunwald E, McCabe CH, Horvath I, Keltai M, Herrman JP, et al; TRITON-TIMI 38 Investigators.
Intensive oral antiplatelet therapy for reduction of ischaemic events including
stent thrombosis in patients with acute coronary syndromes treated with
percutaneous coronary intervention and stenting in the TRITON-TIMI 38 trial: a
subanalysis of a randomised trial. Lancet. 2008;371(9621):1353-63.
20. Ge L, Airoldi F, Iakovou I, Cosgrave J, Michev I,
Sangiorgi GM, et al. Clinical and angiographic outcome after implantation of drug-eluting
stents in bifurcation lesions with the crush stent technique: importance of
final kissing balloon postdilation. J Am Coll Cardiol. 2005;46(4):613-20.
Recibido:
12 de enero de 2012
Aceptado
para su publicación: 27 de febrero de 2012